
Pascale Marchot
Directrice de recherche émérite
Responsable du thème Neurobiologie structurale de l’équipe
Thèse Univ Aix-Marseille-II (maintenant Aix-Marseille Univ.)
HDR Univ. de la Méditerrannée (maintenant Aix-Marseille Univ.)
DR1 CNRS émérite
Vice-présidente de la SFET


Domaines d’Investigation
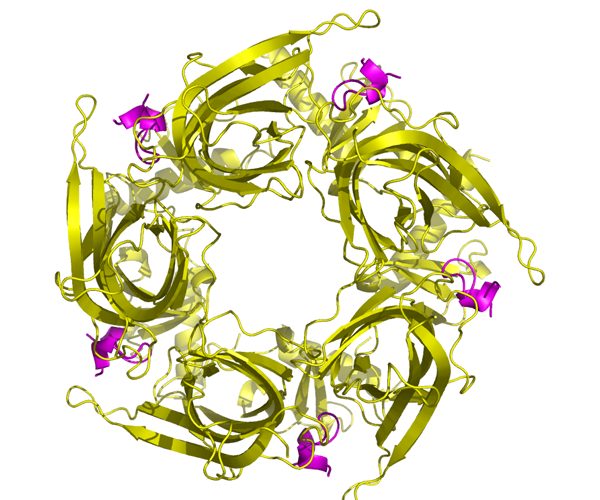
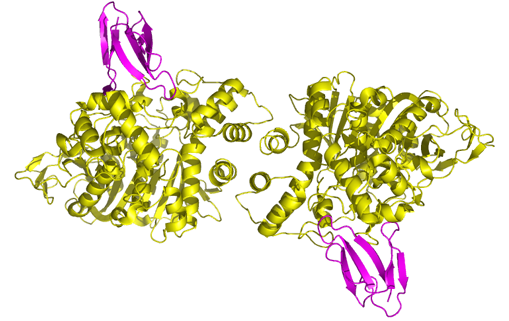
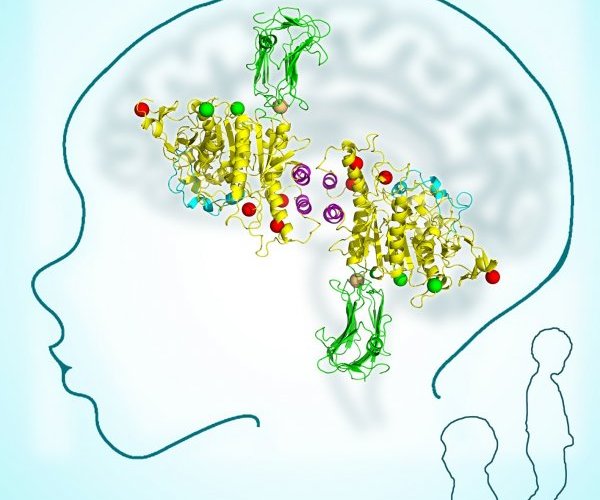
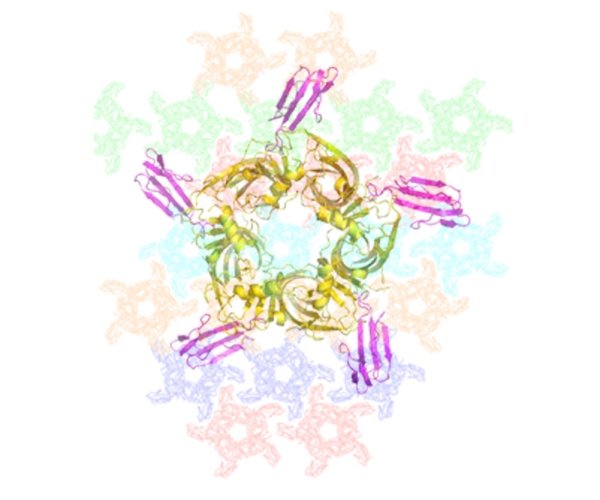
Mes recherches s’adressent aux relations structure-fonction de toxines animales, enzymes, récepteurs/canaux et molécules d’adhésion cellulaire qui sont d’un intérêt neurobiologique considérable de par leur(s) implication(s) dans la genèse, la physiologie, la pathologie ou le vieillissement des structures synaptiques centrales ou périphériques. Mes objectifs sont de documenter (i) les bases moléculaires et structurales de ces récepteurs et molécules d’adhésion et celles de la réactivité et la spécificité de leurs partenaires peptidiques ou organiques ; (ii) les mécanismes moléculaires et événements dynamiques associés à la formation et la stabilisation du complexe et conduisant à une modification de l’activité de ces récepteurs et molécules d’adhésion.
Mots clé : Biochimie, pharmacologie, enzymologie et toxinologie moléculaires – Activité et structure de molécules biologiques – Neurosciences et neurobiologie – Physiologie, pathologie et vieillissement de la synapse.
Parcours
- 2014 – actuel : Co-responsable (avec Yves Bourne) de l’équipe Neurobiologie et Glycobiologie Structurales, labo AFMB, Marseille
- 2013 – 2016 : Responsable français du Laboratoire International Associé « SGIDSTS » (CNRS/AMU/UCSD) (responsable US : Palmer Taylor)
- 2012 – 2013 : Responsable du thème Neurobiologie Structurale, équipe Neurobiologie et Glycobiologie Structurales, labo Architecture et Fonction des Macromolécules Biologiques (AFMB), Marseille
- 2008 – 2011 : Responsable de l’équipe Toxines Animales et Cibles Macromoléculaires (ToxCiM), labo CRN2M, Marseille
- 2000 – 2007 : Responsable de l’équipe Réactivité et Structure de Macromolécules Biologiques, labo Ingénierie des Protéines/BIMC, Marseille
- 2012 – actuel : Chercheur CNRS statutaire, labo Architecture et Fonction des Macromolécules Biologiques (AFMB), Marseille
- 1996 – 2011 : Chercheur CNRS statutaire, labos Ingénierie des Protéines, puis Biologie des Interactions Moléculaires et Cellulaires (BIMC), puis Centre de Recherches en Neurobiologie et Neurophysiologie de Marseille (CRN2M), Marseille (même labo, différents noms).
- 1994 – 1995 : Chercheur CNRS statutaire, séjour sabbatique 2 ans auprès du Dept. Pharmacology, UCSD, La Jolla CA (Etats-Unis)
- 1989 – 1993 : Chercheur CNRS statutaire, labo Biochimie – Ingénierie des Protéines, Marseille
- 1988, 15 octobre: Recrutement CNRS
- 1987 – 1988 : Post-doc, labo Biochimie – Ingénierie des Protéines, Marseille
- 1983 – 1986 : DEA + Thèse Sp. Neurosciences Moléculaires, labo de Biochimie, Marseille
Diplômes universitaires
- 1999 – Habilitation à Diriger les Recherches (HDR), sp. Neurosciences, Univ. Méditerranée, Marseille « Fasciculines et acétylcholinestérase, une histoire d’atomes crochus ». Jury: Cassian Bon, Jacques Grassi, André Nieoullon, Hervé Rochat, Herman van Tilbeurgh, Robert Verger.
- 1986 – Thèse Univ. Aix-Marseille II, sp. Neurosciences, Marseille « Contribution à l’étude de la purification et du mode d’action des toxines des venins de serpents Elapidae ». Directeur de thèse: Hervé Rochat; encadrant: Pierre E. Bougis. Jury: Pierre Fromageot, François Miranda, Hervé Rochat, Rolland Rosset.
- 1983 – Diplôme d’Etudes Approfondies (DEA, maintenant Master-2), sp. Biologie Cellulaire et Moléculaire, Univ. Aix-Marseille II « Chromatographie d’immunoaffinité anti-phospholipase A2 et iodation d’une cardiotoxine du venin de Naja mossambica mossambica« . Directeur: Hervé Rochat; encadrant: Pierre E. Bougis.
Prix
- 2017 : Nomination pour le Club-M-Ambassadeurs de la Ville de Marseille
- 2017 : Trophée de l’Attractivité – Congrès de la Ville de Marseille, pour y avoir organisé le XVe Symposium International sur les Mécanismes Cholinergiques (XVth ISCM) en 2016
- 2016 : B.P. Doctor Memorial Young Investigator Travel Award, honoris causa
- 2013-2016 : Prime d’Excellence Scientifique (PES) du CNRS
Conseils, Comités, Jurys
Conseils et comités
- Toxins (MDPI), Editorial Board Member, en cours.
- Integrative Structural Biology Meeting 2023 (BSI-2023, Marseille, France), Comité d’organisation.
- « Supervisor » MSCA Postdoctoral Fellowship et « advisor » CIVIS 3i pour le laboratoire AFMB, depuis 2021.
- Participante/membre du European Venom Network (EUVEN) Groupes de Travail WG1 « Novel targets in venom research », WG4 « Web ressources » et WG5 « Training », 2021-2025.
- Volontaire de l’Infrastructure Nationale de Recherche et cohorte épidémiologique Constance, depuis 2018
- J. Biol. Chem., membre du comité éditorial, 2016-2021.
- GTBio 2014, comité scientifique, membre sollicité.
- XIV-th ISCM (2013, Chine), 12-th ChE (2015, Espagne), XV-th ISCM (2016, Marseille, France): Comités d’organisation et Conseils consultatifs internationaux, membre élu.
- Société Française pour l’Etude des Toxines (SFET), Conseils scientifique et d’administration, Bureau, Comité d’Organisation des Colloques, Comité d’Édition, membre élu depuis 2007; vice-présidente depuis 2025.
- Vaincre la Mucoviscidose (VLM, ex- AFLM), Conseil Scientifique et Bureau, membre élu 2002 – 2008.
Jurys thèse et HDR
- Stéphanie Simon, Laboratoire de Neurobiologie Cellulaire et Moléculaire, ENS, Paris, mai 1999, « Structure fonctionnelle de l’acétylcholinestérase: mise en évidence d’un nouveau site régulateur – organisation des oligomères », Thèse de Doctorat de l’Univ. Pierre et Marie Curie (Paris VI), sp. Siences de la vie – Pharmacologie moléculaire et cellulaire. En tant que examinateur, auprès de Jean-Pierre Toutant et Richard Rotundo (rapporteurs), Jacques Grassi (examinateur), Michel Morange (président), Jean Massoulié (directeur de thèse).
- Stéphanie Antil-Delbeke, DIEP, CEA Saclay, Gif-sur-Yvette, octobre 2000, « Quels sont les mécanismes moléculaires impliqués dans la spécificité d’interaction de neurotoxines pour les récepteurs nicotiniques de type musculaire et neuronal alpha7? », Thèse de Doctorat de l’Univ. René Descartes (Paris V), Discipline: Sciences pharmaceutiques, sp. Pharmacologie moléculaire, pharmacologie expérimentale, métabolisme. En tant que rapporteur, auprès de Hugues Bedouelle (rapporteur), Daniel Bertrand, Pierre-Jean Corringer, André Ménez (examinateurs), Christiane Garbay (présidente), Denis Servent (directeur de thèse).
- Carole Fruchart-Gaillard, DIEP, CEA Saclay, Gif-sur-Yvette, juin 2003, « Caractérisation pharmacologique et structurale de l’interaction de neurotoxines sur des récepteurs cholinergiques », Thèse de Doctorat de l’Univ. Paris VI, sp. Biologie cellulaire et moléculaire. En tant que rapporteur, auprès de Jean-Louis Galzi (rapporteur), Pierre Nicolas et André Ménez (examinateurs), Denis Servent (directeur de thèse).
- Ludovic Renault, Laboratoire d’Ingénierie des Protéines, IFR Jean Roche, Marseille, déc 2005, « Approche structurale de l’inhibition de l’acétylcholinestérase par des anticorps monoclonaux », Thèse de Doctorat de l’Univ. de la Méditerranée, sp. Neurosciences. En tant que directeur de thèse, auprès de Jean Massoulié et Herman van Tilbeurgh (rapporteurs), Jacques Grassi et Yves Bourne (examinateurs), Alain Enjalbert (président).
- Noël Perrier, Laboratoire de Neurobiologie, ENS, Paris, déc 2005, « Expression et accumulation fonctionnelle de l’acétylcholinestérase dans le système nerveux central », Thèse de Doctorat de l’Univ. René Descartes (Paris V), Discipline Sciences de la Vie et de la Matière, sp. Biologie de la cellule normale et pathologique. En tant que rapporteur, auprès de Nicolas Morel (rapporteur), Michèle Garlatti et Jacques Mallet (examinateurs), Pierre-Olivier Couraud (président), Jean Massoulié (directeur de thèse).
- Séverine Marconi, Neurobiologie des Canaux Ioniques, IFR Jean Roche, Marseille, nov 2008, « Dosage de l’activité endoprotéolytique de neurotoxines clostridiales », Thèse de Doctorat de l’Univ. de la Méditerranée, sp. Neurosciences. En tant que examinateur, auprès de Marie-Bernadette Villiers et Michel R. Popoff (rapporteurs), Claire Dane et Christian Lévêque (examinateurs), Alain Enjalbert (président), Nicole Moutot (directeur de thèse).
- Grégoire Mondielli, équipe ToxCiM, CRN2M, IFR Jean Roche, Marseille, déc 2011, « Étude fonctionnelle de l’acétylcholinestérase : régulation de la catalyse par la région de la porte arrière et recherche d’un partenaire non-catalytique endogène – Mise en évidence et caractérisation d’une nouvelle cible de la fasciculine, distincte de l’acétylcholinestérase », Thèse de Doctorat de l’Univ. de la Méditerranée, sp. Neurosciences. En tant que directeur de thèse auprès de Eric Krejci et Denis Servent (rapporteurs), Stéphanie Simon (examinateur), Hervé Darbon (examinateur et président).
- Guillaume Blanchet, équipe Toxines, Récepteurs et Canaux, Service d’Ingénierie Moléculaire des Protéines (DSV/iBiTEC-S/SIMOPRO), CEA Saclay, Gif sur Yvette, oct 2013, « Pharmacologie, phylogénie et ingénierie moléculaire des toxines aminergiques du venin de mamba ciblant les RCPG amines biogènes », Thèse de Doctorat de l’Univ. Paris VI, sp. Biologie cellulaire et moléculaire. En tant que rapporteur, auprès de Brigitte Ilien (rapporteur), Sylvie Diochot et Thierry Foulon (examinateurs), Manolo Gouy (président), Denis Servent (directeur de thèse).
- Lamia Mebarki, équipe Glycobiologie et neurobiologie structurales, laboratoire AFMB et SARL BioXtal/Theranyx, Marseille, oct 2017, « Recherche ou développement, et caractérisation fonctionnelle et structurale d’effecteurs peptidiques de deux récepteurs membranaires à incidences physiopathologiques », Thèse de Doctorat de l’Univ. Aix-Marseille, discipline Biologie, sp. Biochimie structurale. En tant que directeur de thèse auprès de Ghérici Hassaine (co-directeur de thèse), Denis Servent et Jean-Louis Baneres (rapporteurs), Pierre Edouard Bougis (examinateur), James Sturgis (examinateur et président), Sylvie Diochot (invitée).
- Rana El Masri, équipe Structure et Activité des Glycosaminoglycanes, Institut de Biologie Structurale, Grenoble, sept 2019, « Functional and structural characterization of human endosulfatase HSulf-2 », Thèse de Doctorat de la Communauté Univ. Grenoble Alpes, sp. Biologie structurale et nanobiologie. En tant que rapporteur, auprès de Kenji Uchimura (rapporteur), Régis Daniel (examinateur), Nicole Thielens (examinateur et président), Romain Vivès (directeur de thèse).
- Ophélie Da Silva, Institut de Recherche Biomédicale des Armées (IRBA), Dépt. de Toxicologie et Risques Chimiques, Unité Neurotoxiques, Brétigny-sur-Orge, déc 2021, « Etudes enzymatiques et structurales de réactivateurs de l’acétylcholinestérase inhibée par des neurotoxiques organophosphorés », Thèse de Doctorat de l’Univ. Paris-Saclay, ED Innovation thérapeutique : du fondamental à l’appliqué (ITFA), sp. Biochimie et biologie structurale. En tant que rapporteur, auprès de Luc Belzunces (rapporteur), Julie Mennetrey et Jacques-Philippe Colletier (examinateurs), Herman Van Tilbeurgh (examinateur et président), Florian Nachon et José Diaz (co-directeurs de thèse).
- Jonathan Elegheert, équipe Neurobiologie structurale, interactions et ingénierie protéique des récepteurs, Interdisciplinary Institute for NeuroScience (IINS), Univ. Bordeaux, Centre Broca Nouvelle Aquitaine, Bordeaux, mai 2024, “Structural biology and engineering of neuronal proteins”, HDR de l’Univ. Bordeaux. En tant que examinateur, auprès de Laetitia Mony, Hugues Nury, Fekrije Selimi (rapporteurs), Pierre-Jean Corringer (examinateur et président).
- Anushka Nair, équipe Neurobiologie structurale, interactions et ingénierie protéique des récepteurs, IINS, Univ. Bordeaux, Centre Broca Nouvelle Aquitaine, Bordeaux, sept 2025, “Nanobody discovery and affinity engineering approaches for targeting ionotropic glutamate receptors”, Doctorat de l’Univ. Bordeaux. En tant que rapporteur, auprès de Miriam Stoeber et Rob Meijers (rapporteurs), Derrick Robinson (examinateur), Sébastien Fribourg (examinateur et président), Jonathan Elegheert (directeur de thèse).
- Arnaud Billet, labo BTSB, INU Jean-François Champollion, Albi, déc 2025, « Peptides issus de venins de fourmis : identification et caractérisation fonctionnelle des peptides et de leurs mécanismes d’action », HDR de l’Univ. Paul Sabatier-Toulouse III. En tant que examinateur, auprès de Aurélien Chatelier, Pierre Charnet et Christian Legros (rapporteurs) et Elsa Bonnafé (directrice d’HDR).
Sociétés
- Association de Cristallographie d’Aix-Marseille (ACAM) : 2013 – 2023
- Association Française de Cristallographie (AFC) : 2012 – 2023
- Association pour l’Etude des Cholinestérases : depuis 1996 (n’est plus active)
- Association pour la Recherche sur la Sclérose Latérale Amyotrophique & autres maladies du motoneurone (ARSla) : 2007 – 2018
- Association pour les Femmes en Science et en Ingénierie (AFSI) : depuis 2015 (n’est plus active)
- Club -M- Ambassadeurs de la Ville de Marseille : 2017 – 2020 (n’est plus active)
- Société des Neurosciences (SN) (associée à la International Brain Research Organization (IBRO) et la Federation of European Neuroscience Societies (FENS)) : 2011 – 2022
- Société Française d’Endocrinologie (SFE) : 2018
- Société Française de Biophysique (SFB) : 2016, 2018
- Société Française pour l’Etude des Toxines (SFET) : membre depuis 1999, membre du CA depuis 2007, vice-présidente depuis 2025
- American Society for Biochemistry and Molecular Biology (ASBMB) (associée à la International Union of Biochemistry and Molecular Biology (IUBMB)) : 2012 – 2021
- International Society for Neurochemistry (ISN) : 2015 – 2018
- International Society on Toxinology (IST) : 2007 – 2020
- Society for Neuroscience (SfN) : 2013 – 2018
- National Geographic Society USA : 1994 – 2008
Collaborations
- AgroM Différenciation Cellulaire et Croissance (INRA) et Unité Informatique de Centre INRA, Montpellier, France
- Laboratoire de Neurobiologie Cellulaire et Moléculaire, CNRS, Institut Fédératif de Neurobiologie Alfred Fessard, Gif-sur-Yvette, France
- Laboratoire de Toxinologie Moléculaire, Service d’Ingénierie Moléculaire des Protéines, Institut de biologie & de technologies de Saclay, CEA, Gif-sur-Yvette, France
- Institut Interdisciplinaire de Neuroscience (IIN), CNRS/Univ Bordeaux2, Centre de Génomique Fonctionnelle, Bordeaux, France
- Société BioXtal, campus Luminy, Marseille, France
- Lab Synapse Biology, VIB Center for the Biology of Disease, KU Leuven, Center for Human Genetics, Leuven, Belgium
- Skaggs School of Pharmacy and Pharmaceutical Sciences (SSPPS), Dept of Pharmacology, University of California at San Diego (UCSD), La Jolla, CA, USA
- Dept of Neuroscience and Cell Biology, UMDNJ-Robert Wood Johnson Medical School, Child Health Institute of New Jersey, New Brunswick, NJ, USA
- Dept of Chemistry and Biochemistry, University of California at Santa Barbara (UCSB), Santa Barbara, CA, USA
- Institut NeuroMyoGene, Univ Claude Bernard Lyon 1/CNRS/INSERM, Villeurbanne
- Unité de Neurobiologie des canaux Ioniques et de la Synapse (UNIS), INSERM, Marseille
- Institut du Développement de Marseille (IBDM), CNRS/AMU, Marseille
- Institut de Pharmacologie Moléculaire et Cellulaire (IPMC), CNRS/U Côte d’Azur, Sophia-Antipolis
- Centre de Recherche en Cancérologie de Marseille (CRCM), Inserm/CNRS/AMU/IPC), Marseille
Financements d’études et de recherches
- 1982 (1 mois, sept) : Vacations sur contrat CNRS.
- 1982-1983 (1 an) : Bourse de Diplôme d’Etudes Approfondies (DEA, maintenant Master-2).
- 1983-1986 (3 ans, oct-sept) : Bourse de Recherche du Ministère de la Recherche et Technologie (MRT) pour élaboration d’une Thèse d’Université.
- 1984 : Allocation d’Information Scientifique et Technique (BIST) du Ministère de la Recherche et Technologie (MRT) – Mission Interministérielle de l’Information Scientifique et Technique (MIDIST).
- 1987 (1 an, jan-déc): Bourse de soudure, Fondation pour la Recherche Médicale (FRM).
- 1988 (5 mois, jan-mai) : Vacations sur contrat de la Direction des Recherches et Etudes Techniques (DRET) de la Délégation Générale pour l’Armement (DGA).
- 1988-1989 (1 an, juin-mai) : Contrat de Recherche temporaire du CNRS (renonciation au 15 oct 1988 suite à recrutement permanent).
- 1994 (9 mois) : CNAM – OTAN, bourse complémentaire d’études à l’étranger pour chercheur confirmé.
- 1995 (10 mois) : Salaire de « Visiting Scholar », Dept. Pharmacology, UCSD, la Jolla, CA.
- 1997-1999 (3 ans) : ACI CNRS-NSF, P Marchot et P Taylor (UCSD, La Jolla, CA) coordonnateurs.
- 1997-1999 (3 ans) : AFM, P Marchot et PE Bougis (CNRS Marseille) coordonnateurs.
- 2000-2002 (3 ans) : PAI franco-allemand PROCOPE, P Marchot et O Pongs (ZMNH, Hambourg) coordonnateurs.
- 2001-2002 (2 ans) : AFM, P Marchot coordonnateur.
- 2003-2004 (2 ans) : Programme Bioinformatique inter EPST, P Marchot et A Chatonnet (INRA Montpellier) coordonnateurs.
- 2003-2004 (2 ans) : AFM, P Marchot coordonnateur.
- 2005-2007 (3 ans) : Action CNRS/USA, P Marchot et P Taylor (UCSD, La Jolla, CA) coordonnateurs.
- 2005 (1 an) : AFM, P Marchot coordonnateur.
- 2006-2008 (3 ans) : GIP-ANR Santé-environnement – Santé-travail, partenaire.
- 2006-2009 (48 mois) : Project Intégré Structural Proteomics in Europe SPINE2-COMPLEXES and TEACH-SG, Work Package WP1.3.1, partner 14 ; Y Bourne (CNRS Marseille) coordonnateur, P Marchot deputy.
- 2009 (1 an) : PEPS INSB-CNRS, MF Martin-Eauclaire (CNRS Marseille) coordonnateur ; P Marchot, PE Bougis, B Céard participants.
- 2010-2012 (3 ans) : PICS CNRS, P Marchot et Y Bourne coordonnateurs ; P Taylor (UCSD, La Jolla, CA) partenaire.
- 2011-2014 (45 mois) : ANR-Blanc SVSE 2 – Progr Biologie cellulaire & développement, coordonnateur.
- 2013-2016 (4 ans) : CNRS INSB, LIA franco-américain SGIDSTS, P Marchot et P Taylor (UCSD, La Jolla, CA) coordonnateurs.
- 2014-2017 (3,5 ans) : ANR-Blanc SVSE 4 – Progr Neurosciences, partenaire.
- 2015-2019 (4 ans) : ANR – Progr Exploration du système nerveux dans son fonctionnement normal et pathologique (DS0407), partenaire
- 2017-2022 (5 ans) : ANR – Progr Vie, santé et bien-être (DS04), partenaire.
- 2024-2026 (3 ans): ANR – Projets Génériques, CE11, coordonateur.
LIA SGIDSTS
La convention pour la création d’un Laboratoire International Associé (LIA) entre le laboratoire Architecture et Fonction des Macromolécules Biologiques (AFMB) à Marseille, France, et le Palmer Taylor laboratory, Skaggs School of Pharmacy and Pharmaceutical Sciences (SSPPS) à La Jolla, Californie, a été signée par les institutions françaises Centre National de la Recherche Scientifique (CNRS) et Aix-Marseille Université (AMU), et l’institution americaine Université de Californie à San Diego (UCSD), en février-avril 2015. Ce LIA était nommé Structure-Guided Investigations into Disease States and Therapeutic Strategies (acronyme SGIDSTS) et il a de fait commencé à fonctionner le 1er janvier 2013, pour 4 ans. Il était coordonné du coté français par Pascale Marchot, chercheur CNRS, et du coté américain par Palmer Taylor, chercheur et professeur UCSD. Les activités du LIA SGIDSTS concernaient la recherche fondamentale en neuropharmacologie et biochimie structurale. (Voir http://fr.calameo.com/read/00248816… page 7; https://www.nature.com/nature-index/institution-outputs/france/laboratoire-international-associe-structure-guided-investigations-into-disease-states-and-therapeutic-strategies-lia-sgidsts/5971647f140ba0fb368b456b ; https://www.cnrs.fr/CNRS-Hebdo/provence-corse/Lettre/343/Lettre.aspx ; https://www.univ-amu.fr/system/files/2019-02/DIRCOM-lettre_amu_n17_janv2014.pdf pages 17-18; https://www.france-science.com/IMG/pdf/rapport_activite_mst_2013.compressed.pdf pages 80-81.)
Assistances expérimentales
- Joan R. Kanter, staff research associate UCSD, 1994-1995 (maintenant « Faculty Admin Assistant » dans le « Roger Tsien Lab », UCSD)
- Marianick Juin, technicienne CNRS (statutaire), 2000-2005 (maintenant technicienne à l’Institut Méditerranéen de Biodiversité et d’Ecologie Marine et Continentale – IMBE-, campus Arbois, Aix-en-Provence)
- Sandrine Conrod, technicienne CNRS (statutaire), 2005-2011 (ensuite technicienne à l’Institut de Neurophysiopathologie de Marseille, maintenant technicienne au Centre Européen de Recherche et d’Enseignement en Géosciences de l’Environnement – CEREGE – à Aix-en-Provence)
- Claire Debarnot, ingénieure d’études AMU (statutaire), 2010-2011 (maintenant membre du labo AFMB et de notre équipe, depuis jan 2017)
- Audrey Blanchard, ingénieure d’études, 2011-2014 (maintenant ingénieure à Innate Pharma, Marseille)
- Supanee (« Ann ») Potisopon, ingénieure de recherche/postdoc, oct-déc 2014 (ensuite postdoc à Harvard Medical School, Boston, MA ; maintenant ingénieure chez BIOASTER, Lyon)
- Aurélien Assice-Vivoni, ingénieur d’études, sept 2015 (maintenant alternant chargé de mission qualité hygiène sécurité et environnement pour EDF)
- Julie Baptiste, ingénieure d’études, nov 2015 – sept 2016 (ensuite ingénieure à l’Institut de Génétique Humaine, Montpellier ; maintenant ingénieure chez Sys2Diag, Montpellier)
- Maria Mate, ingénieure de recherche CNRS (statutaire), oct 2013 – mai 2017 (maintenant membre d’une autre équipe du laboratoire AFMB)
- Marie-Julie Dejardin, ingénieure d’études, oct 2016 – juin 2017 (maintenant ingénieure à l’Institut NeuroMyoGene (INMG), Lyon)
- Jean-Baptiste Boitel, ingénieur d’études, fév 2018 – nov 2019 (ensuite : ingénieur au Laboratoire Adhésion et Inflammation (LIA), Campus Luminy, Marseille, en collaboration avec une autre équipe du laboratoire AFMB ; maintenant cadre de laboratoire chez Sanofi (Montpellier)
- Marine Papin, ingénieure d’études, sept 2020 – fév 2021 (maintenant étudiante en thèse à Dijon)
Etudiant.e.s, post-doctorant.e.s, visiteurs.euses
Stagiaires
- Rozenn Guegan, Maitrise Biologie Cellulaire & Physiologie, Univ Rennes, avr – juin 1998, puis DEA Neurosciences, Univ de la Méditerranée, sept – nov 1998 (abandon)
- Céline Hamel, BTS Ecole Nationale de Chimie Physique & Biologie, Paris, mai – juil 1999 & mars 2000
- Romain Morichon, Licence Biochimie, Univ Franche-Comté, UFR Sciences & Techniques, Besançon, juin – août 2000
- Ludovic Renault, Magistère de l’Univ de Rouen (3e année) et DEA Biochimie Biologie Structurale et Génomique, Univ Aix-Marseille, sept 2001- juin 2002
- Raja Noufir (maintenant Bonifay), BTS Lycée Pro Marie Curie, Marseille, mai – juin 2003 & nov – déc 2003 (2 x 8 sem)
- Virginie Fabre, 4e année INSA de Lyon, Dépt Biosciences, juin – juil 2004 (8 sem)
- Audrey Luzergues, 2e année ESIL, Dépt Génie Biologique & Microbiologie Appliquée, Marseille, fév – avr 2005 (8 sem)
- Marion Traverse, 2e année ESIL, Dépt Génie Biologique & Microbiologie Appliquée, Marseille, mars – avr 2006 (8 sem)
- Carole Rosenberger, Master-1 Nutrition – Sécurité Alimentaire, option Biochimie, Univ Méditerranée, Marseille, avr – juin 2006 (8 sem)
- Delphine Chaduli, BTS Lycée Pro Marie Curie, Marseille, mai – juin 2006 & oct – déc 2006 (2 x 8 sem)
- Grégoire Mondielli, Master-2 Neurosciences, Univ Méditerranée, jan – juin 2007
- David Menahem, 2e année ESIL, Dépt Biotechnologie, Marseille, fév – avr 2010 (8 sem.)
- Pauline Dressayre, 2e année ESIL, Dépt Biotechnologie, Marseille, fév – avr 2011 (8 sem) (co-encadrement G Mondielli)
- Julie Prats, 2e année ESIL, Dépt Biotechnologie, Marseille, fév – avr 2012 (8 sem) (co-encadrement A Blanchard)
- Camille Ribeyre, Master-1 Biochimie Biologie Structurale et Génomique (BBSG), Aix-Marseille Univ, avr – mai 2013 (8 sem) (co-encadrement A Blanchard)
- Florian Mourey, 2e année AgroParisTech, Institut des sciences & industries du vivant & de l’environnement, Centre de Paris, juin-juil 2014 (8 sem) (co-encadrement A Goulet)
- Farida Nezlioui, Master-2 Biochimie Biologie Structurale et Génomique (BBSG), Aix-Marseille Univ, jan – juin 2016 (co-encadrement A Goulet)
- Yoann Crétinon, Master-1 Biochimie Biologie Structurale et Génomique (BBSG), Aix-Marseille Univ, mar – avr 2017 (7 sem) (co-encadrement A Goulet, S Platsaki)
- Melvin Boumedour, BTS Lycée La Forbine, Marseille, mai-juil (6 sem) et nov-déc 2017 (8 sem) (encadrement principal S Platsaki)
- Sarah Coulibaly Martineau, Master-2 Biologie Structurale, Génomique (BSG), Aix-Marseille Univ, jan-juin 2019 (co-encadrement C Debarnot)
- Djouhaina Benmehidi, 2e année Sup’Biotech Paris, juin-juillet 2019 (8 sem) (encadrement principal S Platsaki)
- Nafisatou Drame, Master-2 Biologie Structurale, Génomique (BSG), Aix-Marseille Univ, jan-juin 2021 (6 mois) (co-encadrement C Debarnot)
- Cynthia Lohberger, Master-1 Biologie Structurale, Génomique (BSG), Aix-Marseille Univ, avr-mai 2021 (7 sem) (co-encadrement C Debarnot)
- Cynthia Lohberger, Master-2 Biologie Structurale, Génomique (BSG), Aix-Marseille Univ, jan-juin 2022 (6 mois) (co-encadrement C Debarnot)
- Malorie Spies, Master-1 Biologie Structurale, Génomique (BSG), Aix-Marseille Univ, avr-mai 2025 (7 sem) (co-encadrement I. Prabudiansyah)
Etudiant.e.s en thèse
- Fatima Laraba-Djebari, Thèse de l’Université d’Aix-Marseille II, sp. Biologie cellulaire et microbiologie, 1993-1995, en co-encadrement (dir. de thèse : Marie-France Martin-Eauclaire).
- Actuellement : Doyenne de la Faculté des Sciences Biologiques, Université des Sciences et de la Technologie Houari Boumédiène (FSB-USTHB), Alger, Algérie.
- Ludovic Renault, Thèse Univ Méditerranée, sp. Neurosciences, sept 2002 – déc 2005
- Financements : Association France Alzheimer ; Association Française contre les Myopathies ; Programme Bioinformatique inter-EPST
- Puis : Postdoc Stahlberg Lab, Molecular and Cellular Biology, College of Biological Sciences, Univ California Davis, CA, USA, 2006-2009 / Research associate, Howard Young Lab, Dept Biochemistry, Univ Alberta, Edmonton, Canada, 2009-2012 / Senior scientific officer, Cancer Research UK, London Research Inst, UK, 2013 – 2015
- Puis : Research Scientist & Facility Manager, NeCEN, Leiden University, NL, 2016
- Actuellement : Research Scientist & Head of NeCEN facility, Leiden University, NL, depuis 2018
- Grégoire Mondielli, Thèse Univ Méditerranée, sp. Neurosciences, sept 2007 – déc 2011
- Financements : Association Française contre les Myopathies ; CNRS ; Fondation pour la Recherche Médicale
- Puis : Ingénieur de recherche, CRN2M Marseille, équipe Gliotransmission et Synaptopathies, 2013 – 2016 / équipe SIGnalling in NeuroEndocrine Tumors (SIG-NET), 2016 – 2018
- Actuellement : ingénieur de recherche, Institut de NeuroPhysiopathologie, Marseille Medical Genetics, équipe DIP-NET, depuis 2018 (voir https://fr.linkedin.com/in/gregoire…)
- Lamia Mebarki, Thèse Aix-Marseille Univ, sp. Biologie Structurale et Biochimie, nov 2013 – oct 2017
- Financement : BioXtal nov 2013 – mars 2014 ; CIFRE-ANRT BioXtal-AFMB avr 2014 – mars 2017 ; Theranyx avr – juin 2017 ; AFMB juil – dec 2017
- Puis : Ingénieure R&D, Promise Advanced Proteomics, Grenoble, jan-mai 2019
- Actuellement : Chef de Projet, Covalab, Lyon, mai 2019 – en cours
Post-doctorant.e.s
- Igor Fabrichny, suite à Thèse Univ Lomonosov Moscou (RU) 1995-1999 puis 1er postdoctorat au Institute of Biotechnology, Univ Helsinki (FI) 2000-2005
- Financements : CNRS « Proposition d’accueil pour un post-doctorant au CNRS » oct 2005 – sept 2006 ; Fondation pour la Recherche Médicale « Accueil de post-doctorant étranger » oct 2006 – sept 2008
- Actuellement : Chef de Produits, International Biotechnology Center GENERIUM, Volginskiy RU, 2011 – en cours
- Adeline Goulet, suite à (i) Thèse Univ Aix-Marseille au laboratoire AFMB 2006-2009, (ii) 1er postdoctorat au CBS Montpellier 2009-2010, puis (iii) 2nd postdoctorat au Birkbeck College à Londres (UK) 2010-2013
- 3e postdoctorat dans notre équipe ; financement Fondation pour la Recherche Médicale, sept 2013 – sept 2015
- Ensuite : Chercheur CNRS (CR2) dans notre équipe, oct 2015 – sept 2017
- Actuellement : Chercheur CNRS (CR2) AFMB équipe Interactions hôte-pathogène, depuis sept 2017
- Semeli Platsaki, suite à (i) Thèse en Biochimie des Protéines, Institute for Cell and Molecular Biosciences, Newcastle Univ (UK) 2010-2015, puis (ii) 1er postdoctorat au Northern Institute for Cancer Research, Newcastle Univ (UK) 2015-2016
- 2e postdoctorat dans notre équipe ; financement ANR juin 2016 – sept 2019 plus PRESTIGE (actions Marie Skłodowska-Curie, Campus France) sept 2017 – sept 2018.
- 3e postdoctorat dans l’équipe Génétique et neurobiologie de C. elegans, INM, Lyon, avec mise à disposition dans notre équipe, financement ANR nov 2019 – jan 2020.
- Ensuite: 4e postdoctorat dans l’équipe Réplicases virales : structure, mécanisme, et drug-design du laboratoire AFMB, Marseille, financement Janssen avril – nov 2020.
- Actuellement: employée par l’European Virus Archive – GLOBAL (EVAg), Marseille
Visiteurs/euses long terme
- Sventja von Daake, visiteur Dept of Pharmacology, UCSD, nov 2003 – oct 2004
- Financement : Pharmacology Education Research Foundation
- Ensuite : Research associate, Susan Taylor Lab, UCSD, La Jolla, CA, USA
- Ensuite : Lab manager, Comoletti Lab, Dept Neuroscience and Cell Biology, UMDNJ-RWMS, Child Health Institute of New Jersey, New Brunswick, NJ, USA
- Actuellement : Staff Scientist Cytomics Specialist, Malaghan Institute of Medical Research, Wellington, New Zealand
- Nicolas Lenfant, post-doctorant visiteur, convention d’accueil Dynamique Musculaire & Métabolisme, INRA, Montpellier, juin 2011 – déc 2013
- Financement : ANR
- Ensuite : post-doctorant AFMB équipe Glycogénomique, jan 2014 – déc 2016
- Actuellement : ingénieur au Marseille Medical Genetics, Faculté de Médecine Timone, Marseille, mars 2018 – en cours
- Nafisatou Drame, ingénieure hébergée, convention d’accueil entre Tafalgie Therapeutics SAS et le laboratoire AFMB, oct 2021 – avr 2024
- Financement : CDD Tafalgie Therapeutics SAS
- Ensuite : ingénieure CDI Tafalgie Therapeutics SAS, Marseille, avril 2024 – en cours
Autres stagiaires & visiteurs/euses
- Kael Duprey, stagiaire UCSD, juin-oct 1994 & juin-oct 1995 (aux US)
- Claudine N. Prowse, stagiaire UCSD, jan 1994 – déc 1995 (aux US)
- Verena Pollmann, visiteur PhD Univ Hambourg (dir de thèse : O. Pongs), mars 2000 & juin 2000 (2 & 1 sem)
- Jens Dannenberg, visiteur Postdoc Institut fuer Neurale Signalverarbeitung, ZMNH, Hamburg, oct 2001 (2 sem)
- Scott B. Hansen, visiteur PhD UCSD (dir de thèse, Palmer Taylor), avr – juin 2004 & nov – déc 2004 (7 & 8 sem)
- Ryan Hibbs, visiteur Postdoc UCSD, nov – déc 2006
- Cécile Tardif & Marion Leblanc, classe 1ère S, Lycée des Pierres Vives, Carrières-sur-Seine, déc2013 – mars2014, exclusivement par courriel !
Publications originales et revues
1986
Bougis PE, Marchot P, Rochat H (1986) Characterization of Elapidae snake venom components using optimized reverse-phase high performance liquid chromatographic conditions and screening assays for α-neurotoxin and phospholipase A2 activities. Biochemistry 25, 7235-7243.
1987
Bougis PE, Marchot P, Rochat H (1987) In vivo synergy of cardiotoxin and phospholipase A2 from the Elapid snake Naja mossambica mossambica. Toxicon 25, 427-431.
Martin MF, Rochat H, Marchot P, Bougis PE (1987) Use of high performance liquid chromatography to demonstrate quantitative variation in components of venom from the scorpion Androctonus australis Hector. Toxicon 25, 569-573.
Otting G, Marchot P, Bougis PE, Rochat H, Wüthrich K (1987) Monitoring the purification by high performance liquid chromatography of cardiotoxins from Naja mossambica mossambica using phase-sensitive two dimensional nuclear magnetic resonance. Eur J Biochem 168, 603-607.
1988
Marchot P, Bougis PE, Céard B, Van Rietschoten J, Rochat H (1988) Localization of the toxic site of Naja mossambica mossambica cardiotoxins : small synthetic peptides express an in vivo lethality. Biochem Biophys Res Comm 153, 642-647.
Marchot P, Frachon P, Bougis PE (1988) Selective distinction at equilibrium between the two α-neurotoxin binding sites of Torpedo acetylcholine receptor by microtitration. Eur J Biochem 174, 537-542.
Zeghloul S, Marchot P, Bougis PE, Ronin C (1988) Selective loss of binding sites for the iodinated α-neurotoxin I from Naja mossambica mossambica upon enzymatic deglycosylation of Torpedo electric organ membranes. Eur J Biochem 174, 543-550.
1989
Le Du MH, Marchot P, Bougis PE, Fontecilla-Camps JC (1989) Crystals of fasciculin 2 from green mamba snake venom : preparation and preliminary X-ray analysis. J Biol Chem 264, 21401-21402.
1990
Muniz ZM, Tibbs GR, Marchot P, Bougis PE, Nicholls DG, Dolly JO (1990) Homologues of a K+ channel blocker α-dendrotoxin : characterization of synaptosomal binding sites and their coupling to elevation of cytosolic free calcium concentration. Neurochem Int 16, 105-112.
Gourdou I, Mabrouk K, Harkiss G, Marchot P, Watt N, Hery F, Vigne R (1990) Neurotoxicité chez la souris de portions riches en cystéines des protéines Tat du virus visna et de VIH-1 [en français ; résumé en anglais]. C R Acad Sci (Paris) 311, Série III, pp. 149-155.
1992
Le Du MH, Marchot P, Bougis PE, Fontecilla-Camps JC (1992) 1.9 Å resolution structure of fasciculin 1, an anti-acetylcholinesterase toxin from green mamba snake venom. J Biol Chem 267, 22122-22130.
Laraba-Djebari F, Martin-Eauclaire MF, Marchot P (1992) A fibrinogen-clotting serine proteinase from Cerastes cerastes (horned viper) venom with arginine-esterase and amidase activities : purification, characterization and kinetic parameter determination. Toxicon 30, 1399-1410.
1993
Marchot P, Khélif A, Ji YH, Mansuelle P, Bougis PE (1993) Binding of 125I-fasciculin to rat brain acetylcholinesterase : the complex still binds diisopropyl fluorophosphate. J Biol Chem 268, 12458-12467.
1995
van den Born HKL, Radić Z, Marchot P, Taylor P, Tsigelny I (1995) Theoretical analysis of the structure of the peptide fasciculin and its docking to acetylcholinesterase. Protein Sci 4, 703-715.
Laraba-Djebari F, Martin-Eauclaire MF, Mauco G, Marchot P (1995) Afaâcytin, an αβ-fibrinogenase from Cerastes cerastes (Horned Viper) venom, activates purified factor X and induces serotonin release from human blood platelets. Eur J Biochem 233, 756-765.
Bourne Y, Taylor P, Marchot P (1995) Acetylcholinesterase inhibition by fasciculin : crystal structure of the complex. Cell 83, 503-512.
Taylor P, Radić Z, Hosea NA, Camp S, Marchot P, Berman HA (1995) Structural bases for the specificity of cholinesterase catalysis and inhibition. Toxicol Lett 82-83, 453-458.
1996
Le Du MH, Housset D, Marchot P, Bougis PE, Navaza J, Fontecilla-Camps JC (1996) Crystal structure of fasciculin 2 from green mamba snake venom : evidence for unusual loop flexibility. Acta Cryst D52, 87-92.
Marchot P, Ravelli RBG, Raves ML, Bourne Y, Vellom DC, Kanter J, Camp S, Sussman JL, Taylor P (1996) Soluble monomeric acetylcholinesterase from mouse : expression, purification, and crystallization in complex with fasciculin. Protein Sci 5, 672-679.
1997
Marchot P, Prowse CN, Kanter J, Camp S, Ackermann EJ, Radić Z, Bougis PE, Taylor P (1997) Expression and inhibitory activity of mutants of fasciculin, a peptidic acetylcholinesterase inhibitor from mamba venom. J Biol Chem 272, 3502-3510.
1998
Sugiyama N, Marchot P, Kawanishi C, Osaka H, Molles B, Sine S, Taylor P (1998) Residues at the subunit interfaces of the nicotinic acetylcholine receptor that contribute to α-conotoxin M1 binding. Molec Pharmacol 53, 787-794.
Marchot P, Bourne Y, Prowse CN, Bougis PE, Taylor P (1998) Highlights in toxin research – Inhibition of mouse acetylcholinesterase by fasciculin : crystal structure of the complex and mutagenesis of fasciculin. Toxicon 36, 1613-1622.
Taylor P, Osaka H, Molles BE, Sugiyama N, Marchot P, Malany S, McArdle JJ, Sine SM, Tsigelny I (1998) Toxins selective for subunit interfaces as probes of nicotinic acetylcholine receptor structure. J Physiol (Paris) 92, 79-83.
1999
Bourne Y, Taylor P, Bougis PE, Marchot P (1999) Crystal structure of mouse acetylcholinesterase : a peripheral site-occluding loop in a tetrameric assembly. J Biol Chem 274, 2963-2970.
Sentjurc M, Pecar S, Stojan J, Marchot P, Radić Z, Grubič Z (1999) Electron paramagnetic resonance reveals altered topography of the active site gorge of acetylcholinesterase after binding of fasciculin to the peripheral site. Biochem Biophys Acta 1430, 349-358.
Bourne Y, Grassi J, Bougis PE, Marchot P (1999) Conformational flexibility of the acetylcholinesterase tetramer revealed by X-ray crystallography. J Biol Chem 274, 30370-30376.
Marchot P (1999) L’interaction fasciculine-acétylcholinestérase [Monographie en français ; résumé en anglais]. J Soc Biol 193, 505-508.
2000
Tricaud N, Marchot P, Martin-Eauclaire MF (2000) On the kaliotoxin and dendrotoxin binding sites on rat brain synaptosomes. Toxicon 38, 1749-1758.
2001
Bourne Y, Dannenberg J, Pollmann V, Marchot P, Pongs O (2001) Immunocytochemical localization and crystal structure of human frequenin (neuronal calcium sensor 1). J Biol Chem 276, 11949-11955.
2002
Tai K, Shen T, Henchman RH, Bourne Y, Marchot P, McCammon JA (2002) Mechanism of acetylcholinesterase inhibition by fasciculin : a 5 ns molecular dynamics simulation. J Am Chem Soc 124, 6153-6161.
Geib S, Sandoz G, Mabrouk K, Matavel A, Marchot P, Hoshi T, Villaz M, Ronjat M, Miquelis R, Lévêque C, De Waard M (2002) Use of a purified and functional recombinant Ca2+ channel β4 subunit in surface plasmon resonance studies. Biochem J 364, 285-292.
2003
Bourne Y, Taylor P, Radić Z, Marchot P (2003) Structural insights into ligand interactions at the acetylcholinesterase peripheral anionic site. EMBO J 22, 1-12.
2004
Hotelier T, Renault L, Cousin X, Nègre V, Marchot P, Chatonnet A (2004) ESTHER, the database of the α/β-hydrolase fold superfamily of proteins. Nucleic Acids Res 32, D145-147.
Bourne Y, Kolb HC, Radić Z, Sharpless KB, Taylor P, Marchot P (2004) Freeze-frame inhibitor captures acetylcholinesterase in a unique conformation. Proc Natl Acad Sci USA 101, 1449-1454.
Bourne Y, Hasper AA, Chahinian H, Juin M, de Graaff LH, Marchot P (2004) Aspergillus niger protein EstA defines a new class of fungal esterases within the α/β-hydrolase fold family of proteins. Structure (Camb) 12, 677-687 [Erratum in Structure (Camb) 12, 1545]. (See also Preview “Defining substrate characteristics from 3D structure : perspective on EstA structure” by Schrag JD & Cygler M, Structure (Camb) 12, 521-522.)
2005
Legros C, Céard B, Vacher H, Marchot P, Bougis PE, Martin-Eauclaire MF (2005) Expression of the scorpion α-toxin of reference AaH-II and mutants for identification of some key bioactive elements. Biochem Biophys Acta 1723, 91-99.
Bourne Y, Talley TT, Hansen SB, Taylor P, Marchot P (2005) Crystal structure of a Cbtx-AChBP complex reveals essential interactions between snake α-neurotoxins and nicotinic receptors. EMBO J 24, 1512–1522 [Corrigendum in EMBO J. 25, 266 (2006)].
Hansen SB, Sulzenbacher G, Huxford T, Marchot P, Taylor P, Bourne Y (2005) Structures of Aplysia AChBP complexes with nicotinic agonists and antagonists reveal distinctive binding interfaces and conformations. EMBO J 24, 3635–3646.
Bourne Y, Radić Z, Kolb HC, Sharpless KB, Taylor P, Marchot P (2005) Structural insights into conformational flexibility at the AChE peripheral site and active site gorge [Revue]. Chem Biol Interact 157-158, 159-165.
Renault L, Nègre V, Hotelier T, Cousin X, Marchot P, Chatonnet A (2005) New friendly tools for users of ESTHER, the database of the α/β-hydrolase fold superfamily of proteins. Chem Biol Interact 157-158, 339-343.
Bourne Y, Hasper AA, Chahinian H, Renault L, Juin MA, de Graaff LH, Marchot P (2005) A. niger protein « EstA », perhaps a new electrotactin, defines a new class of fungal esterases within the α/β-hydrolase fold superfamily. Chem Biol Interact 157-158, 395-396.
Renault L, Essono S, Boquet D, Juin M, Grassi J, Bourne Y, Marchot P (2005) Structural insights into AChE inhibition by monoclonal antibodies. Chem Biol Interact 157-158, 397-400.
2006
Bourne Y, Radić Z, Sulzenbacher G, Kim E, Taylor P, Marchot P (2006) Substrate and product trafficking through the active center gorge of acetylcholinesterase analyzed by crystallography and equilibrium binding. J Biol Chem 281, 29256-29267.
Hansen SB, Sulzenbacher G, Huxford T, Marchot P, Bourne Y, Taylor P (2006) Structural characterization of agonist and antagonist-bound acetylcholine-binding protein from Aplysia californica. J Mol Neurosci 30 (1-2), 101-102.
Bourne Y, Hansen SB, Sulzenbacher G, Talley TT, Huxford T, Taylor P, Marchot P (2006) Structural comparison of three crystalline complexes of a peptidic toxin with a synaptic acetylcholine recognition protein. J Mol Neurosci 30 (1-2), 103-104.
Hansen S, Sulzenbacher G, Huxford T, Marchot P, Bourne Y, Taylor P (2006) Conformational states of AChBP revealed by X-ray crystal structures of bound nAChR agonists, antagonists and non-competitive ligands. Acta Pharmacol Sin 27, 390-390.
2007
Fabrichny IP, Leone P, Sulzenbacher G, Comoletti D, Miller MT, Taylor P, Bourne Y, Marchot P (2007) Structural analysis of the synaptic protein neuroligin and its β-neurexin complex : determinants for folding and cell adhesion. Neuron 56, 979-991. (See also Preview “A Crystal-Clear Interaction : Relating Neuroligin/Neurexin Complex Structure to Function at the Synapse” by Levinson J.N. & El-Husseini A. Neuron 56, 937-939.)
2009
Hibbs RE*, Sulzenbacher G*, Shi J, Talley TT, Conrod S, Kem WR, Taylor P, Marchot P, Bourne Y (2009) Structural determinants for interaction of partial agonists with acetylcholine binding protein and neuronal α7 nicotinic acetylcholine receptor. EMBO J 28, 3040-3051. (*Co-1ers auteurs.)
2010
Bourne Y, Radić Z, Aráoz R, Talley TT, Benoit E, Servent D, Taylor P, Molgó J, Marchot P (2010) Structural determinants in phycotoxins and AChBP conferring high affinity binding and nicotinic AChR antagonism. Proc Natl Acad Sci USA 107, 6076-6081.
Leone P, Comoletti D, Ferracci G, Conrod S, Garcia SU, Taylor P, Bourne Y, Marchot P (2010) Structural insights into the exquisite selectivity of neurexin/neuroligin synaptic interactions. EMBO J 29, 2461-2471.
Leone P, Comoletti D, Taylor P, Bourne Y, Marchot P (2010) Structure-function relationship of the α/β-hydrolase fold domain of neuroligin : a comparison with acetylcholinesterase [Revue]. Chem Biol Interact 187, 49–55.
Hotelier T, Nègre V, Marchot P, Chatonnet A (2010) Insecticide resistance through mutations in cholinesterases or carboxylesterases : data mining in ESTHER database. J Pestic Sci 35, 315-320.
Bourne Y, Radić Z, Taylor P, Marchot P (2010) Conformational remodeling of femtomolar inhibitor-acetylcholinesterase complexes in the crystalline state. J Am Chem Soc 132, 18292-18300.
2012
Marchot P, Chatonnet A (2012) Editorial to the Special Issue on “Hydrolase versus other functions of members of the α/β-hydrolase fold superfamily of proteins”. Protein Peptide Lett 19, 130-131.
Marchot P, Chatonnet A (2012) Enzymatic activity and protein interactions in α/β-hydrolase fold proteins : moonlighting versus promiscuity. In : Special Issue on “Hydrolase versus other functions of members of the α/β-hydrolase fold superfamily of proteins”. Protein Peptide Lett 19, 132-143.
Fabrichny IP, Mondielli G, Conrod S, Martin-Eauclaire MF, Bourne Y, Marchot P (2012) Structural insights into antibody sequestering and neutralizing of Na+-channel α-type modulator from Old World scorpion venom. J Biol Chem 287, 14136-14148.
2013
Lenfant N, Hotelier T, Velluet E, Bourne Y, Marchot P, Chatonnet A (2013) ESTHER, the database of the α/β-hydrolase fold superfamily of proteins : tools to explore diversity of functions. Nucleic Acids Res (Database Issue) 41, D423-D429.
Lenfant N, Hotelier T, Bourne Y, Marchot P, Chatonnet A (2013) Proteins with an α/β-hydrolase fold : relationships between subfamilies in an ever-growing superfamily. Chem Biol Interact 203, 266-268.
Martin-Eauclaire MF, Benoit E, Marchot P, Barbier J, Molgó J, Servent D (2013) Editorial to the Special Issue on “Toxins : From Threats to Benefits” (Molgó J, Benoit E, Barbier J, Marchot P, Servent D, Guest Eds), Toxicon 75, 1-2.
Bourne Y*, Renault L*, Essono S, Mondielli G, Lamourette P, Boquet D, Grassi J, Marchot P (2013) Molecular characterization of monoclonal antibodies that inhibit acetylcholinesterase by targeting the peripheral site and backdoor region. PLOS One 8, e77226. (*Co-1ers auteurs.)
2014
Lenfant N, Hotelier T, Bourne Y, Marchot P, Chatonnet A (2014) Tracking the origin and divergence of cholinesterases and neuroligins : the evolution of synaptic proteins. J Mol Neurosci 53, 362-369.
Bourne Y, Marchot P (2014) The neuroligins and their ligands: from structure to function at the synapse. J Mol Neurosci 53, 387-396.
Benoit E, Mattei C, Barbier J, Marchot P, Molgó J, Servent D (2014) Editorial to the Special Issue on “Freshwater and Marine Toxins” (Molgó J, Benoit E, Barbier J, Marchot P, Servent D, Guest Eds), Toxicon 91, 1-4.
2015
Bourne Y*, Renault L*, Marchot P (2015) Crystal structure of snake venom acetylcholinesterase in complex with inhibitory antibody fragment Fab410 bound at the peripheral site : evidence for open and closed states of a back door channel. J Biol Chem 290, 1522–1535. (*Co-1ers auteurs.)
Bourne Y, Sulzenbacher G, Radić Z, Aráoz R, Reynaud M, Benoit E, Zakarian A, Servent D, Molgó J, Taylor P, Marchot P (2015) Marine macrocyclic imines, pinnatoxins A and G : structural determinants and functional properties to distinguish neuronal α7 from muscle (α1)2βγδ nAChRs. Structure 23, 1106-1115. (See also Preview « From Shellfish Poisoning to Neuroscience » by Shahsavar A and Balle T, Structure 23, 979-980.)
2016
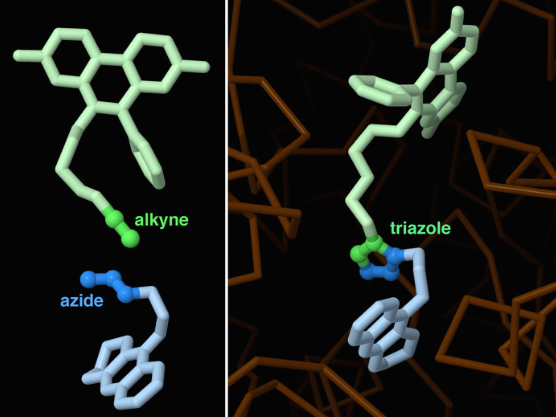
Bourne Y, Sharpless KB, Taylor P, Marchot P (2016) Steric and dynamic parameters influencing in situ cycloadditions to form triazole inhibitors with crystalline acetylcholinesterase. J Am Chem Soc 138, 1611−1621.
Lenfant N, Bourne Y, Marchot P, Chatonnet A (2016) Relationships of human α/β hydrolase fold proteins and other organophosphate-interacting proteins. Chem Biol Interact 259, 343-351.
2017
Prado MAM, Marchot P, Silman I (2017) Preface to the Special Issue « Cholinergic Mechanisms ». J Neurochem 142 Suppl 2, 3-6.
Kessler P, Marchot P, Silva M, Servent D (2017) The three-finger toxin fold : a multifunctional structural scaffold able to modulate the cholinergic functions. J Neurochem 142 Suppl 2, 7-18.
Molgó J, Marchot P, Aráoz R, Benoit E, Iorga BI, Zakarian A, Taylor P, Bourne Y, Servent D (2017) Cyclic imine toxins from dinoflagellates : a growing family of potent antagonists of the nicotinic acetylcholine receptors. J Neurochem 142 Suppl 2, 41-51.
Chatonnet A, Lenfant N, Marchot P, Selkirk ME (2017) Natural genomic amplification of cholinesterase genes in animals. J Neurochem 142 Suppl 2, 73-81.
Thoumine O, Marchot P (2017) A triad of crystals sheds light on MDGA interference with neuroligation. Neuron 95, 729-731.
2018
Bourne Y, Marchot P (2018) Hot spots for protein partnership at the surface of cholinesterases and related alpha/beta hydrolase fold proteins or domains – a structural perspective. Molecules 23, 35.
2019
Chatonnet A, Brazzolotto X, Hotelier T, Lenfant N, Marchot P, Bourne Y (2019) An evolutionary perspective on the first disulfide bond in members of the cholinesterase-carboxylesterase (COesterase) family : Possible outcomes for cholinesterase expression in prokaryotes. Chem Biol Interact 308, 179-184.
2020
Trobiani L, Meringolo M, Diamanti T, Bourne Y, Marchot P, Martella G, Dini L, Pisani A, De Jaco A, Bonsi P (2020) The neuroligins and the synaptic pathway in Autism Spectrum Disorder (Review). Neurosci Biobehav Rev 119, 37-51.
Platsaki S, Zhou X, Pinan-Lucarré B, Delauzun V, Tu H, Mansuelle P, Fourquet P, Bourne Y, Bessereau J-L, Marchot P (2020) The Ig-like domain of Punctin/MADD-4 is the primary determinant for interaction with the ectodomain of neuroligin NLG-1. J Biol Chem 295, 16267-16279.
2021
Comoletti D, Trobiani L, Chatonnet A, Bourne Y, Marchot P (2021) Comparative mapping of selected structural determinants on the extracellular domains of cholinesterase-like cell-adhesion molecules (Review). Special Issue on ‘Acetylcholinesterase Inhibitors’ (Guest Editor, Maria Braga). Neuropharmacology 184, 108381.
2022
Ramirez-Franco J, Debreux K, Extremet J, Maulet Y, Belghazi M, Villard C, Sangiardi M, Youssouf F, El Far L, Lévêque C, Debarnot C, Marchot P, Paneva S, Debanne D, Russier M, Seagar M, Irani SR, El Far O (2022) Patient-derived antibodies reveal the subcellular distribution and heterogeneous interactome of LGI1. Brain 145, 3843-3858.
2023
Chatonnet A, Perochon M, Velluet E, Marchot P (2023) The ESTHER database on alpha/beta hydrolase fold proteins – An overview of recent developments. Chem Biol Interact 383, 110671.
Martin-Eauclaire MF, Marchot P (2023) Obituary – Hervé Paul Marie Antoine ROCHAT 1937–2023. Toxicon 233, 107249.
2024
Bourne Y, Sulzenbacher G, Chabaud L, Aráoz R, Radić Z, Conrod S, Taylor P, Guillou C, Molgó J, Marchot P (2024) The cyclic imine core common to the marine macrocyclic toxins is sufficient to dictate nicotinic acetylcholine receptor antagonism. Mar. Drugs 22, 149. [This article belongs to the Special Issue ‘Marine Biotoxins 2.0’ of Marine Drugs (Molgo J., Guest ed).]
Zancolli G*, von Reumont BM*, Anderluh G, Caliskan F, Chiusano ML, Fröhlich J, Hapeshi E, Hempel BF, Ikonomopoulou MP, Jungo F, Marchot P, Mendes de Farias T, Modica MV, Moran Y, Nalbantsoy A, Procházka Y, Tarallo A, Tonello F, Vitorino R, Zammit ML, Antunes A (2024) Web of venom: exploration of big data resources in animal toxin research. GigaScience 13, giae054. (*Co-1ers auteurs.)
2025
Jenner R*, Anderluh G, Antunes A, Caliskan F, Damm M, Gruber CW, Hempel BF, Holford M, Ikonomopoulou M, Kekeçoğlu M, Kirchhoff K, Kool J, Lakušić M, Ben Mansour R, Marchot P, Modica MV, Nalbantsoy A, Oukkache N, Požek K, von Reumont BM, Sarigiannis Y, Tarallo A, Tonello F, Vitorino R, Vrenozi B, Zammit ML (2025) Syllabus for a Master’s-level course on animal venomics. Zenodo DOI 10.5281/zenodo.15304515.
2026
Dutertre S*, Nicke A*, Ikonomopoulou MP*, Modica MV*, Finol-Urdaneta RK*, Antunes A, Avella I, Ayvazyan N, Belleza OJV, Bocian A, Bosmans F, Caliskan F, Černecká L, Codreanu I, Codreanu M, Damm M, Djilani S, Dugon MM, Fusi F, Gajski G, Galindo JC, Gilles N, Gruber CW, Hucho T, Igci N, Jungo F, Koludarov I, Lakušić M, Lissoni A, Louchene C, Lüddecke T, Marchot P, Muttenthaler M, Nalbantsoy A, Perpétuo L, von Reumont BM, Rui V, Saponara S, Yiannis Sarigiannis Y, Denis Servent D, Harald H. Sitte H, Manuel Tenorio M, Nataša Tomašević N, Tonello F, Vrenozi B, Khai Khun Yap M. Venom Peptide Pharmacology: The Good, The Bad, And The Not-So-Ugly. Pharmacol Rev, soumis. (*Co-1ers auteurs.)
Production éditoriale
Ouvrage Toxines & cancer (Goudey-Perrière F, Benoit E, Goyffon M, Marchot P, eds) Coll. Rencontres en Toxinologie, Editions Lavoisier, Cachan, 2006 (326 pages) (ISBN : 2-7430-0958-6).
Ouvrage Toxines émergentes : nouveaux risques (Goudey-Perrière F, Benoit E, Marchot P, Popoff M, eds) Coll Rencontres en Toxinologie, Editions Lavoisier, Cachan, 2007 (208 pages) (ISBN : 978-2-7430-1037-9).
Ouvrage électronique (e-book) Toxines & fonctions cholinergiques neuronales & non neuronales (Benoit E, Goudey-Perrière F, Marchot P, Servent D, eds) Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, 2008 (160 pages) (ISSN : 1760-6004).
Ouvrage électronique (e-book) Toxines & signalisation (Benoit E, Goudey-Perrière F, Marchot P, Servent D, eds) Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, 2009 (206 pages) (ISSN : 1760-6004).
Ouvrage électronique (e-book) Advances and new technologies in toxinology (Barbier J, Benoit E, Marchot P, Mattei C, Servent D, eds) Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, 2010 (184 pages) (ISSN : 1760-6004).
Numéro Spécial Hydrolase versus other functions of members of the α/β-hydrolase fold superfamily of proteins (Chatonnet A, Marchot P, Guest eds). Protein & Peptide Letters, Bentham Science Publishers Ltd., 2012, vol 19(2), pp 130-197 (ISSN : 0929-8665).
Numéro Spécial Toxins : From Threats to Benefits, 20th Meeting of the French Society of Toxinology (SFET) (Molgó J, Benoit E, Barbier J, Marchot P, Servent D, Guest eds), Toxicon (ISSN : 0041-0101), Elsevier, 2013, vol 75, pp 1-224.
Numéro Spécial Freshwater and Marine Toxins, 21th Meeting of the French Society of Toxinology (SFET) (Molgó J, Benoit E, Barbier J, Marchot P, Servent D, Guest eds), Toxicon (ISSN : 0041-0101), Elsevier, 2014, vol 91, pp 1-184.
Numéro Spécial Cholinergic Mechanisms (Silman I, Guest ed ; Marchot P, Prado MAM, Assoc Guest eds), J Neurochem (ISSN : 1471-4159), Wiley, 2017, vol 142 – Suppl 2, pp 1-226.
Numéro Spécial Toxins : From the Wild to the Lab, 29th Meeting of the French Society of Toxinology (SFET) (Marchot P, Benoit E, Diochot S, Guest eds). Toxins (ISSN: 2072-6651), MDPI, 2024.
Numéro Spécial Unlocking the Deep Secrets of Toxins, 30th Meeting of the French Society of Toxinology (SFET) (Marchot P, Diochot S, Comte K, Popoff MR, Guest eds). Toxins (ISSN: 2072-6651), MDPI, 2025.
Chapitres d’ouvrages & actes de colloques
Marchot P, Bougis PE, Céard B, Van Rietschoten J, Rochat H (1989) Lethal synthetic peptides as models of the toxic site of Naja mossambica mossambica cardiotoxins. In Second Forum on Peptides (Aubry A, Marraud M, Vitoux B, eds) Colloque INSERM / John Libbey Eurotext Ltd 174, 461-464.
Le Du MH, Marchot P, Bougis PE, Fontecilla-Camps JC (1993) Fasciculin 1 (Green mamba). In Macromolecular Structures (Hendrickson WA, Wüthrich K, eds) pp. 152-153, Current Biology Ltd, Philadelphia.
Marchot P, Camp S, Radić Z, Bougis PE, Taylor P (1995) Structural determinants of fasciculin specificity for acetylcholinesterase. In Enzymes of the Cholinesterase Family (Quinn DM, Balasubramanian AS, Doctor BP, Taylor P, eds) pp. 197-202, Plenum Publishing Corp, NY.
Bourne Y, Taylor P, Marchot P (1996) Acetylcholinesterase, recombinant monomeric form (mouse) / fasciculin 2 (mamba) complex. In Macromolecular Structures (Hendrickson WA, Wüthrich K, eds) pp. 8-9, Current Biology Ltd, London, UK.
Bourne Y, Taylor P, Kanter JR, Bougis PE, Marchot P (1998) Crystal structure of mouse acetylcholinesterase. In Structure and Function of Cholinesterases and Related Proteins (Doctor BP, Taylor P, Quinn DM, Rotundo RL, Gentry MK, eds) pp. 315-322, Plenum Publishing Corp, NY.
Marchot P, Bourne Y, Prowse CN, Kanter JR, Eads J, Bougis PE, Taylor P (1998) Fasciculin inhibition of mouse acetylcholinesterase : crystal structure of the complex and mutagenesis of fasciculin. In Structure and Function of Cholinesterases and Related Proteins (Doctor BP, Taylor P, Quinn DM, Rotundo RL, Gentry MK, eds) pp. 331-338, Plenum Publishing Corp., NY.
Kanter JR, Eads J, Camp S, Marchot P, Taylor P (1998) Expression and purification of recombinant mutants of fasciculin from mammalian cells. In Structure and Function of Cholinesterases and Related Proteins (Doctor BP, Taylor P, Quinn DM, Rotundo RL, Gentry MK, eds) pp. 240-241, Plenum Publishing Corp, NY.
Marchot P, Bougis PE (2000) The fasciculins, and their interaction with acetylcholinesterase. In : Animal Toxins. Facts and Protocols (Rochat H, Martin-Eauclaire MF, eds) pp. 246-275, Birkhäuser Verlag, Basel.
Bourne Y, Marchot P (2002) Fasciculines et autres ligands de l’AChE : développements structuraux récents [Revue en français ; résumé en anglais]. In : Toxines et Recherches Biomédicales (Goudey-Perrière F, Bon C, Puiseux-Dao S, Sauviat MP, eds) pp. 287-296, Coll. Rencontres en Toxinologie, Editions Scientifiques et Médicales Elsevier, Paris.
Comoletti D, Flynn R, Jennings L, Hoffman R, Marchot P, Bourne Y, Südhof T, Taylor P (2004) Interaction of recombinant soluble neuroligin-1 with neurexin-1-β. In Cholinergic Mechanisms – function and dysfunction Symposium Proceedings (Silman I, Michaelson DM, Anglister L, Fisher A, Soreq H, eds) pp. 523-525, Taylor & Francis group, UK.
Tai K, Shen T, Henchman RH, Bourne Y, Marchot P, McCammon JA (2004) Mechanism of acetylcholinesterase inhibition by fasciculin : A 5ns molecular dynamics simulation. In Cholinergic Mechanisms – function and dysfunction Symposium Proceedings (Silman I, Michaelson DM, Anglister I, Fisher A, Soreq H, eds) pp. 727-728, Taylor & Francis group, UK.
Bourne Y, Hansen SB, Sulzenbacher G, Talley TT, Huxford T, Taylor P, Marchot P (2005) Comparaison structurale de trois complexes entre une toxine peptidique et une protéine synaptique liant l’acétylcholine. [Revue en français ; résumé en anglais]. In Toxines et Douleur (Bon C, Goudey-Perrière F, Goyffon M, Sauviat MP, eds), pp. 213-216, Coll Rencontres en Toxinologie, Editions Lavoisier, Cachan, France.
Fabrichny I, Conrod S, Martin-Eauclaire MF, Devaux C, Bourne Y, Marchot P (2007) Immunothérapie antiscorpionique : approche structurale. [En français ; résumé & légendes en anglais]. In Toxines émergentes : nouveaux risques (Goudey-Perrière F, Benoit E, Marchot P, Popoff M, eds), pp. 197-202, Coll Rencontres en Toxinologie, Editions Lavoisier, Cachan, France.
Bourne Y, Radić Z, Talley TT, Conrod S, Taylor P, Molgó J, Marchot P (2008) Utilisation des « protéines liant l’ACh » (AChBP) en toxinologie structurale : nouveaux exemples. [En français ; résumé & légendes en anglais]. In Toxines et fonctions cholinergiques neuronales et non neuronales (Benoit E, Goudey-Perrière F, Marchot P, Servent D, eds), pp. 27-28, Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, France.
Taylor P, Radić Z, Talley TT, Nemecz A, De Jaco A, Comoletti D, Fabrichny IP. Leone P, Miller MT, Dubi N, Fokin VV, Sharpless KB, Bourne Y, Marchot P (2008) Retrogenomics – Proceeding from gene product back to the gene : applications in drug discovery and uncovering linkages in congenital disorders. [Revue en anglais ; résumé & légendes en français]. In Toxines et fonctions cholinergiques neuronales et non neuronales (Benoit E, Goudey-Perrière F, Marchot P, Servent D, eds), pp. 29-32, Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, France.
Douzi B, Geerlof A, Gilles N, Darbon H, Marchot P, Vincentelli R (2010) A new system for expressing recombinant animal toxins in E. coli ? In Advances and new technologies in toxinology (Barbier J, Benoit E, Marchot P, Mattei C, Servent D, eds), pp. 149-152, Coll Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, France.
Marchot P, Diochot S, Popoff MR, Benoit E (2020) Report from the 26th Meeting on Toxinology, “Bioengineering of Toxins”, Organized by the French Society of Toxinology (SFET) and Held in Paris, France, 4–5 December 2019. In Special Issue « Selected Papers from the 26th Meeting of the French Society for Toxinology- Bioengineering of Toxins » (Popoff MR, Benoit E, Guest eds). Toxins 12, 31/pp. 1-29. (doi:10.3390/toxins12010031)
Ladant D, Marchot P, Diochot S, Prévost G, Popoff MR, Benoit E (2022) Report from the 27th (Virtual) Meeting on Toxinology, “Toxins : Mr Hyde or Dr Jekyll ?”, Organized by the French Society of Toxinology, 9-10 December 2021. In Special Issue « Toxins : Mr Hyde or Dr Jekyll ? » (Ladant D, Prévost G, Popoff MR, Benoit E, Guest eds). Toxins 14(2), 110/pp. 1-32. (doi: 10.3390/toxins14020110)
Marchot P, Benoit E, Fajloun Z, Diochot S (2023) Report from the 28th Meeting on Toxinology, “Toxins: What’s up, Doc?”, Organized by the French Society of Toxinology on November 28-29, 2022. Toxins 15(2), 126/pp. 1-25. (doi: 10.3390/toxins15020126)
Marchot P, Fajloun Z, Legros C, Benoit E, Diochot S (2024) Report from the 29th Meeting on Toxinology, “Toxins: From the Wild to the Lab”, Organized by the French Society of Toxinology on November 30-December 01, 2023. In Special Issue « Toxins : From the wild to the lab » (Marchot P, Benoit E, Diochot S, Guest eds). Toxins 16, 147/pp. 1-34. (doi: 10.3390/toxins16030147)
Marchot P, Fajloun Z, Benoit E, Diochot S (2025) Report from the 30th Meeting on Toxinology, “Unlocking the Deep Secrets of Toxins”, Organized by the French Society of Toxinology on 2–3 December 2024. In Special Issue « Unlocking the Deep Secrets of Toxins » (Marchot P, Diochot S, Comte K, Popoff MR, Guest eds). Toxins 17, 94/pp. 1-31. (doi: 10.3390/toxins17020094)
Diochot S, Le Garrec R, Dugon MM, Marchot P (2026) Report from the 31st Meeting on Toxinology, “Toxins: Playing with and fighting them!”, Organized by the French Society for Toxinology on December 1-2, 2025. Toxins 18, 138/pp. 1-32. (doi: 10.3390/toxins18030138)
Résumés publiés dans revues à comité de lecture
Bougis PE, Marchot P, Rochat H (1985) Reverse-phase high performance liquid chromatography of Elapidae snake venoms. Toxicon 23, p. 554
Marchot P, Khélif A, Bougis PE (1985) Brain acetylcholinesterase inhibitor from mamba snake venom : reverse-phase HPLC isolation and characterisation. Toxicon 23, p. 592
Marchot P, Bougis PE, Rochat H (1987) High performance liquid chromatography of Elapidae snake venoms. Toxicon 25, p. 372
Laraba-Djebari F, Martin-Eauclaire MF, Marchot P (1993) Two thrombin-like proteinases from Cerastes cerastes (Horn viper) venom : purification, characterization and kinetic parameter determination. Toxicon 31, p. 528
Laraba-Djebari F, Martin-Eauclaire MF, Marchot P (1994) Afaâcytin, a thrombin-like enzyme from the venom of Cerastes cerastes : structural and functional properties. Toxicon 32, p. 400
Marchot P, Khélif A, Ji YH, Mansuelle P, Bougis PE (1994) Binding of 125I-fasciculin to rat brain acetylcholinesterase. Toxicon 32, p. 401
Kanter J, Marchot P, Prowse C, Camp S, Taylor P (1997) Contributions of individual amino acid residues to the stability of the fasciculin-acetylcholinesterase interaction. Pharmacologist 39, p. 104
Marchot P, Taylor P, Kanter JR, Bougis PE, Bourne Y (1998) Tetrameric assembly and peripheral site-occluding loop of mouse acetylcholinesterase. J Physiol (Paris) 92, p. 465
Bougis PE, Taylor P, Marchot P (1998) Biotinylation of the tyrosine residues of fasciculin. J Physiol (Paris) 92, p. 416
Marchot P (1999) Acetylcholinesterase inhibition by fasciculin. Toxicon 37, 1209-1210
Bougis PE, Taylor P, Marchot P (2000) Biotinylated fasciculins : potential tools for histochemical studies of acetylcholinesterase. Toxicon 38, 1637-1638
Flynn R, Comoletti D, Marchot P, Bourne Y, Südhof T, & Taylor P (2003) Interaction of recombinant soluble neuroligins-1 with neurexin-ß. FASEB J. 17 (4), A640
Bourne Y, Sulzenbacher G, Radić Z, Aráoz R, Reynaud M, Benoit E, Talley TT, Zakarian A, Taylor P, Servent D, Molgó J, Marchot P (2014) Diversity in the binding interactions of marine toxins to AChBP, the soluble nAChR surrogate. Toxicon 91, 171-172.
Marchot P, Sharpless KB, Taylor P, Bourne Y (2016) Structural and functional analysis of acetylcholinesterase complexes with “in situ click-chemistry” inhibitors. FASEB J 30 Suppl 1, 833.10.
Bourne Y, Radić Z, Sharpless KB, Taylor P, Marchot P (2017) Structural and functional analysis of acetylcholinesterase complexes with in situ click-chemistry inhibitors. J Neurochem 142 Suppl 2, 189.
Marchot P, Sulzenbacher G, Radić Z, Aráoz R, Reynaud M, Benoit E, Zakarian A, Servent D, Molgó J, Taylor P, Bourne Y (2017) Diversity in the binding interactions of marine phycotoxins to AChBP, the soluble nAChR surrogate. J Neurochem 142 Suppl 2, 196.
Chatonnet A, Marchot P, Bourne Y, Lenfant N, Hotelier T (2017) ESTHER database : update on the alpha/beta hydrolase fold superfamily of proteins. J Neurochem 142 Suppl 2, 209.
Lenfant N, Selkirk ME, Hotelier T, Bourne Y, Marchot P, Chatonnet A (2017) Evolution of animal cholinesterases. J Neurochem 142 Suppl 2, 214.
Chatonnet A, Brazzolotto X, Hotelier T, Lenfant N, Marchot P (2018) Evolution of the first disulfide bond in the cholinesterase-carboxylesterase (coesterase) family: possible consequences for cholinesterase expression in prokaryotes. Mil Med Sci Lett (Voj Zdrav Listy) 87 Suppl 1, 55.
Bourne Y, Sulzenbacher G, Radić Z, Chabaud L, Aráoz R, Benoit E, Zakarian A, Servent D, Guillou C, Taylor P, Molgó J, Marchot P (2020) Diversity in the binding interactions of nicotinic ligands and toxins to the nAChRs and associated conformational fluctuations-Insights into the core motif dictating antagonism. In Marchot P, Diochot S, Popoff MR, Benoit E. Report from the 26th Meeting on Toxinology, « Bioengineering of Toxins », Organized by the French Society of Toxinology (SFET) and Held in Paris, France, 4-5 December 2019. Toxins 12:31, pp. 9-10.
Bourne Y, Sulzenbacher G, Chabaud L, Aráoz R, Radić Z, Conrod S, Taylor P, Guillou C, Molgó J, Marchot P (2024) Is the cyclic imine core common to the marine macrocyclic toxins sufficient to dictate nicotinic acetylcholine receptor antagonism? In Marchot P, Fajloun Z, Legros C, Benoit E, Diochot S. Report from the 29th Meeting on Toxinology, “Toxins: From the Wild to the Lab”, Organized by the French Society of Toxinology on 30 November–1 December 2023. Toxins 16:147, pp. 16-17.
Structures cristallographiques
- 1FAS Fasciculin 1 (LeDu, Marchot, Bougis, Fontecilla-Camps, 1993)
- 1FSC Fasciculin 2 (LeDu, Housset, Marchot, Bougis, Navaza, Fontecilla-Camps, 1995)
- 1MAH Mouse AChE, fasciculin 2 complex (Bourne, Taylor, Marchot, 1995)
- 1KU6 Mouse AChE, revisited fasciculin 2 complex (Bourne, Burmeister, Taylor, Marchot, 2002)
- 1C2B Eel AChE, natural tetramer, structure A (Bourne, Marchot, 1999)
- 1C2O Eel AChE, natural tetramer, structure B (id.)
- 1MAA Mouse AChE, crystalline tetramer (Bourne, Taylor, Bougis, Marchot, 1998)
- 1J06 Mouse AChE, first apo form (Bourne, Taylor, Radić, Marchot, 2002)
- 1J07 Mouse AChE, decidium complex (id.)
- 1N5R Mouse AChE, propidium complex (id.)
- 1N5M Mouse AChE, gallamine complex (id.)
- 2H9Y Mouse AChE, complex with TMTFA (Bourne, Radić, Sulzenbacher, Kim, Taylor, Marchot, 2006)
- 2HA0 Mouse AChE, complex with 4K-TMA (id.)
- 2HA2 Mouse AChE, complex with succinyldicholine (id.)
- 2HA3 Mouse AChE, complex with choline (id.)
- 2HA4 Mouse AChE S203A mutant, complex with acetylcholine (id.)
- 2HA5 Mouse AChE S203A mutant, complex with acetylthiocholine (id.)
- 2HA6 Mouse AChE S203A mutant, complex with succinyldicholine (id.)
- 2HA7 Mouse AChE S203A mutant, complex with butyrylthiocholine (id.)
- 1Q83 Mouse AChE, TZ2PA6 syn1 complex (Bourne, Kolb, Radić, Sharpless, Taylor, Marchot, 2003)
- 1Q84 Mouse AChE, TZ2PA6 anti1 complex (id.)
- 5EHN mouse AChE, syn-TZ2PA5 complex (Bourne, Sharpless, Taylor, Marchot, 2016)
- 5EHQ mouse AChE, anti-TZ2PA5 complex (id.)
- 5EHZ mouse AChE, syn-TZ2PA5 complex from a 1:1 syn/anti mixture (id.)
- 5EIA mouse AChE, anti-TZ2PA5 complex from a 1:6 syn/anti mixture (id.)
- 5EIE mouse AChE, TZ2 complex (id.)
- 5EIH mouse AChE, TZ2+PA5 complex (id.)
- 2XUD Mouse AChE Tyr337Ala mutant (Bourne, Radić, Taylor, Marchot, 2010)
- 2XUG Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 anti1 (1-wk) (id.)
- 2XUF Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 anti1 (1-mth) (id.)
- 2XUH Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 anti1 (10-mths) (id)
- 2XUI Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 syn1 (1-wk) (id)
- 2XUJ Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 syn1 (1-mth) (id)
- 2XUK Mouse AChE Tyr337Ala mutant, cocrystallized complex with TZ2PA6 syn1 (10-mths) (id)
- 2XUO Mouse AChE, Tyr337Ala mutant, soaking complex with TZ2PA6 anti1 (id)
- 2XUP Mouse AChE, Tyr337Ala mutant, soaking complex with TZ2PA6 syn1 (id.)
- 2XUQ Mouse AChE, Tyr337Ala mutant, soaking complex with mixed TZ2PA6 anti1/syn1 (id.)
- 2YMX Inhibitory anti-AChE Fab408 (Bourne, Renault, Essono, Mondielli, Lamourette, Bocquet, Grassi, Marchot, 2013)
- 4QWW Fab410-BfAChE complex (Bourne, Renault, Marchot, 2015)
- 1YI5 Lymnaea AChBP, α-cobratoxin complex (Bourne, Talley, Hansen, Taylor, Marchot, 2005)
- 2BYN Aplysia AChBP, apo (Hansen, Sulzenbacher, Huxford, Marchot, Taylor, Bourne, 2005)
- 2BYP Aplysia AChBP, α-conotoxin Im1 complex (id.)
- 2BYQ Aplysia AChBP, epibatidine complex (id.)
- 2BYR Aplysia AChBP, methyllycaconitine complex (id.)
- 2BYS Aplysia AChBP, lobeline complex (id.)
- 2WNL Aplysia AChBP, anabaseine complex (Hibbs, Sulzenbacher, Shi, Talley, Conrod, Kem, Taylor, Marchot, Bourne, 2009)
- 2WNJ Aplysia AChBP, DMXBA complex (id.)
- 2WN9 Aplysia AChBP, 4-OH-DMXBA complex (id.)
- 2WNC Aplysia AChBP, tropisetron complex (id.)
- 2WZY Aplysia AChBP, SPX complex (Bourne, Radic, Aráoz, Talley, Benoit, Servent, Taylor, Molgo, Marchot, 2010)
- 2X00 Aplysia AChBP, GYM complex (id.)
- 4XHE Aplysia AChBP, PnTx-A complex (Bourne, Sulzenbacher, Marchot, 2015)
- 4XK9 Aplysia AChBP, PnTx-G complex (id.)
- 8Q1M Aplysia AChBP, spiroimine (+)-4 R complex (Sulzenbacher, Bourne, Marchot, 2024)
- 8QTL Aplysia AChBP, spiroimine (–)-4 S complex (id.)
- 8QX2 Aplysia AChBP, spiroimine (±)-4 complex (id.)
- 3BE8 NL4 (Fabrichny, Leone, Sulzenbacher, Comoletti, Miller, Taylor, Bourne, Marchot, 2007)
- 2VH8 Nrxβ1-NL4 complex (id.)
- 2WQZ Nrxβ1-NL4 complex, aternative refinement (replaces 2VH8) 2009
- 2XB6 Revisited Nrxβ1-NL4 complex (Leone, Comoletti, Ferracci, Conrod, Taylor, Bourne, Marchot, 2010)
- 4AEI Fab4C1 bound with scorpion toxin AahII (Fabrichny, Mondielli, Conrod, Martin-Eauclaire, Bourne, Marchot, 2011)
- 4AEH Fab9C2 in the absence of a bound scorpion toxin AahI (id)
- 1G8I Human frequenin (NCS-1) (Bourne, Dannenberg, Pollmann, Marchot, Pongs, 2000)
- 1UKC Aspergillus niger EstA (Bourne, Hasper, Chahinian, Juin, de Graff, Marchot, 2003)
Revues de presse
Pour “Bourne et al., Structure (Camb) 2004” :
“Defining substrate characteristics from 3D structure : perspective on EstA structure” by Schrag JD & Cygler M, Structure (Camb) 12, 521-522.
Pour « Bourne et al., PNAS 2004” :
“Enzyme manufactures its own inhibitor” PNAS News Archive [Feb 2004]
“Sharpless clicks at Informex 2004” Chem. Eng. News 82, 63-65 [Feb 2004] https://cen.acs.org/articles/82/i7/SHARPLESS-CLICKS-INFORMEX-2004.html
“Clicking on to the chemistry of Alzheimer’s” Chem. World 3 [Mar 2004]
“New approach to drug design” UCSD News / Health Sciences [Mar 2004] http://ucsdnews.ucsd.edu/archive/ne…
“Enzyme acetylcholinesterase, new approach to drug design” News-Medical.Net… Medical News [Mar 2004] http://www.news-medical.net/?id=87
“Pharmacologists collaborate on new approach to drug design” MediLexicon/Medical News Headlines [Mar 2004] http://www.pharma-lexicon.com/medic…
« Alzheimer’s enzyme creates its own inhibitor » Chemistry World News / Royal Society of Chemistry [Mar 2004] https://www.chemistryworld.com/news/alzheimers-enzyme-creates-its-own-inhibitor/3000321.article
“Enzymes are doing it for themselves” Biotechniques Euro-edition [Apr 2004]
Pour “Fabrichny et al., Neuron 2007” :
Preview “A Crystal-Clear Interaction : Relating Neuroligin/Neurexin Complex Structure to Function at the Synapse” by Levinson J.N. & El-Husseini A., Neuron 56 (2007) 937-939
“Snapshot of proteins linked to autism”, Royal Society of Chemistry, UK [Dec 2007] http://www.rsc.org/chemistryworld/N…
“Atomic Structure of Proteins Altered in Autism” Newswise [Dec 2007] http://www.newswise.com/articles/vi…
“Study Details Atomic Structure of Proteins Altered in Autism”, UCSD Medical Center [Dec 2007] http://ucsdnews.ucsd.edu/archive/ne…
« L’autisme : un syndrome complexe approché de très près par les chercheurs de l’Université de la Méditerranée et du CNRS : Des protéines neuronales incriminées dans l’autisme vues en 3D », Communiqué de Presse de l’Université de la Méditerrannée [Dec 2007] http://www.univmed.fr/communication…
« Observation en 3D de protéines neuronales incriminées dans l’autisme », Communiqué de presse du CNRS [Dec 2007] http://www2.cnrs.fr/presse/communiq…
« Observation en 3D de protéines neuronales incriminées dans l’autisme », TV5.org – Infos – Les communiqués de presse [Dec 2007] http://www.tv5.org/TV5Site/info/com…
« Observation en 3D de protéines neuronales incriminées dans l’autisme », News Press Le Monde [Dec 2007] http://www.newsfrance.org/communiqu…
« En direct des labos – Autisme : des protéines neuronales incriminées observées en 3D », BE France 203 – Veille technologique internationale, ADIT – Ministère des Affaires Etrangères et Européennes [Jan 2008] http://www.bulletins-electroniques….
“Live from the Labs – 3D Observation of Neuroligins Involved in Autism”, BE France 203 – Veille technologique internationale, ADIT – Ministère des Affaires Etrangères et Européennes [Jan 2008] http://www.bulletins-electroniques….
« Des protéines neuronales incriminées dans l’autisme observées en trois dimensions », Centre de Ressources Autisme Rhône-Alpes, Revue de presse n°22 : 16/12/07 – 31/12/07 [Jan 2008] http://www.cra-rhone-alpes.org/spip…
F1000Prime – Article Recommendations [Feb 2008] [http://f1000.com/prime/1100169]
« Analyse en 3D de protéines neuronales incriminées dans l’autisme », La Lettre de l’Université de la Méditerranée, n°125 Février 2008 p.25 http://www.univmed.fr/communication…
« Observation en 3D de protéines neuronales incriminées dans l’autisme », Paris Presse Actualité [Feb 2008] http://www.parispresse.eu/__n87678_…
« Observation en 3D de protéines neuronales incriminées dans l’autisme », Journal du CNRS, n°218 Mars 2008
« Des protéines incriminées dans l’autisme vues en 3D », Neurosciences – Découvertes en rafale sur le cerveau [Mar 2008] http://www2.cnrs.fr/presse/journal/…
« Pierres fondamentales », Revue de l’UNAPEI, Septembre 2008
Pour “Bourne et al., PNAS 2010” :
« Comment agissent certaines toxines accumulées dans les fruits de mer » [Mar 2010] Communiqué de presse du CNRS http://www2.cnrs.fr/presse/communiq…
« Comment agissent certaines toxines accumulées dans les fruits de mer » [Mar 2010] Communiqué de presse du CEA – Sciences du vivant http://www-dsv.cea.fr/la-dsv/toute-…]
”The mode of action of certain toxins that accumulate in seafood” [Mar 2010] Communiqué de presse du CNRS page internationale http://www2.cnrs.fr/en/1709.htm
« Comment des coquillages deviennent toxiques » [Mar 2010] Ma Planète [http://ma-planete.com/blog/view/id_…]
« Deux toxines des poissons et fruits de mer percées à jour » [Mar 2010] RTL Info [ https://www.rtl.be/art/info/magazine/science-nature/deux-toxines-des-poissons-et-fruits-de-mer-percees-a-jour-156483.aspx ]
« Certains fruits de mer contiennent des toxines provoquant des dysfonctionnements cérébraux » [Mar 2010] Communiqué de presse dans La Dépêche, relayé par Le Quotidien du Médecin [ https://www.ladepeche.fr/article/2010/03/10/793935-certains-fruits-mer-contiennent-toxines-provoquant-dysfonctionnements-cerebraux.html ]
Pour « Bourne et al., Structure 2015” :
Preview « From Shellfish Poisoning to Neuroscience » by Shahsavar A and Balle T, Structure 23, 979-980 [https://www.sciencedirect.com/scien…].
La lettre IBITECS – juin 2015: Synthèse et caractérisation fonctionnelle de phycotoxines marines émergentes [https://joliot.cea.fr/drf/joliot/Pages/ARCHIVES/IBITECS/Actualites/La%20lettre/lettre.aspx?Type=Chapitre&numero=8]
Vulgarisation scientifique
Euromédecine 1987, Montpellier: animation d’un stand et conception et distribution d’une brochure « L’information et la vie – Identification et purification d’une toxine de venin animal ».

Liens d’intérêt
- Base de données ESTHER : https://bioweb.supagro.inrae.fr/ESTHER//
- Société Française pour l’Etude des Toxines : http://sfet.asso.fr/
- International Society on Toxinology : http://www.toxinology.org/
- Society for Neurosciences : http://www.sfn.org/
- Société des Neurosciences : https://www.neurosciences.asso.fr/
- International Society for Neurochemistry: https://www.neurochemistry.org/
- XVth International Symposium on Cholinergic Mechanisms, Marseille, oct 2016 : http://iscm.sciencesconf.org/?lang=fr
- COST Action CA19144 European Venom Network (EUVEN): https://www.cost.eu/actions/CA19144/ et https://euven-network.eu/
- RCSB PDB-101 Molecule of the Month: Acetylcholinesterase: https://pdb101.rcsb.org/motm/54
- RCSB PDB-101 Molecule of the Month: Acetylcholine Receptor: https://pdb101.rcsb.org/motm/71
- RCSB PDB-101 Molecule of the Month: Click Chemistry: https://pdb101.rcsb.org/motm/276
- RCSB PDB-101 Molecular Landscapes: Excitatory and Inhibitory Synapses: https://pdb101.rcsb.org/sci-art/goodsell-gallery/excitatory-and-inhibitory-synapses
- Inhibition de l’acétylcholinestérase par la fasciculine: https://www.youtube.com/watch?v=zLuObW3huks
- Structure of acetylcholinesterases, par Zoran Radic: https://www.youtube.com/watch?v=sKCDx_2s66w
- Acetylcholinesterase: A gorge-ous enzyme: https://www.youtube.com/watch?v=ZrJVVP8Nxtk
- Electric Eel, by Irwin Moon: https://archive.org/details/electric_eel/electric_eel.mpeg
- Les substances actives sur le récepteur nicotinique à l’acétylcholine – Un exemple d’enjeu de préservation de la biodiversité: https://www.pedagogie.ac-nice.fr/svt/productions/html/recepteur-nicotinique-biodiversite/recepteur_nicotinique_biodiversite/index.html
- Naturally Obsessed: The Making of a Scientist: https://drive.google.com/file/d/1uOO9gClGwPYY206N7Y-MCBfYWyP0L3x1/view?usp=sharing
- On Being a Scientist: https://www.youtube.com/watch?v=tCgZSjoxF7c
- Nobel Prize lecture: Barry Sharpless, Chemistry 2022: https://youtu.be/55trnYorBhQ
- Palmer Taylor Research Symposiums at SSPPS, 2016 and 2025: https://pharmacy.ucsd.edu/researchsymposiumhome
- Vidéos des presentations du Symposium 2025: https://pharmacy.ucsd.edu/researchsymposium/symposium-lecture-videos
- Top of the Prots: https://topoftheprots.com/
- Le Monde Sciences Biologie 17 mars 2026: https://www.lemonde.fr/sciences/article/2026/03/17/sur-la-piste-de-l-epibatidine-le-poison-qui-a-tue-alexei-navalny_6671764_1650684.html
Figures de couverture

Ouvrage Structure and Function of Cholinesterases and Related Proteins (Doctor BP, Taylor P, Quinn DM, Rotundo RL, & Gentry MK, eds) Plenum Publishing Corp, NY, 1998 (630 pages) (ISBN : 0-306-46050-5).
Ouvrage électronique (e-book) Toxines et fonctions cholinergiques neuronales et non neuronales (Benoit E, Goudey-Perrière F, Marchot P, Servent D, eds) Coll. Rencontres en Toxinologie, Publications de la SFET, Châtenay-Malabry, 2008 (160 pages) (ISSN : 1760-6004).

Journal J. Am. Chem. Soc. Vol. 132, Iss. 51, December 29, 2010

Special Issue on Cholinergic Mechanisms (Silman I, Guest Ed ; Marchot P, Prado MAM, Assoc Guest Eds), J. Neurochem. Wiley 2017 vol 142 – Suppl 2, pp 1-226 (ISSN : 1471-4159).
Publications
2026
Report from the 31st Meeting on Toxinology, “Toxins: Playing with and Fighting Them!”, Organized by the French Society for Toxinology on 1–2 December 2025
Sylvie Diochot, Raphaële Le Garrec, Michel M Dugon, Pascale Marchot
Toxins 18:138 (2026)10.3390/toxins18030138
2025
Report from the 30th Meeting on Toxinology, "Unlocking the Deep Secrets of Toxins", Organized by the French Society of Toxinology on 2-3 December 2024
Pascale Marchot, Ziad Faljoun, Évelyne Benoit, Sylvie Diochot
Toxins 17:1-31 (2025)10.3390/toxins17020000
2024
Web of venom: exploration of big data resources in animal toxin research
Giulia Zancolli, Björn Marcus von Reumont, Gregor Anderluh, Figen Caliskan, Maria Luisa Chiusano, Jacob Fröhlich, Evroula Hapeshi, Benjamin-Florian Hempel, Maria P Ikonomopoulou, Florence Jungo, Pascale Marchot, Tarcisio Mendes de Farias, Maria Vittoria Modica, Yehu Moran, Ayse Nalbantsoy, Jan Procházka, Andrea Tarallo, Fiorella Tonello, Rui Vitorino, Mark Lawrence Zammit, Agostinho Antunes
GigaScience 13:giae054 (2024)10.1093/gigascience/giae054
The cyclic imine core common to the marine macrocyclic toxins is sufficient to dictate nicotinic acetylcholine receptor antagonism
Yves Bourne, Gerlind Sulzenbacher, Laurent Chabaud, Rómulo Aráoz, Zoran Radić, Sandrine Conrod, Palmer Taylor, Catherine Guillou, Jordi Molgó, Pascale Marchot
Marine drugs 22:149 (2024)10.3390/md22040149
Report from the 29th Meeting on Toxinology, “Toxins: From the Wild to the Lab”, Organized by the French Society of Toxinology on 30 November–1 December 2023
Pascale Marchot, Ziad Fajloun, Christian Legros, Évelyne Benoit, Sylvie Diochot
Toxins 16:147 (2024)10.3390/toxins16030147
2023
Obituary - Hervé Paul Marie Antoine ROCHAT 1937–2023
Marie-France Martin-Eauclaire, Pascale Marchot
Toxicon 233:107249 (2023)10.1016/j.toxicon.2023.107249
The ESTHER database on alpha/beta hydrolase fold proteins - An overview of recent developments
Arnaud Chatonnet, Michel Perochon, Eric Velluet, Pascale Marchot
Chemico-Biological Interactions 383:110671 (2023)10.1016/j.cbi.2023.110671
Report from the 28th Meeting on Toxinology, “Toxins: What’s up, Doc?”, Organized by the French Society of Toxinology on 28–29 November 2022
Pascale Marchot, Évelyne Benoit, Ziad Fajloun, Sylvie Diochot
Toxins 15:1-25 (2023)10.3390/toxins15020126
2022
Patient-derived antibodies reveal the subcellular distribution and heterogeneous interactome of LGI1
Jorge Ramirez-Franco, Kévin Debreux, Johanna Extremet, Yves Maulet, Maya Belghazi, Claude Villard, Marion Sangiardi, Fahamoe Youssouf, Lara El Far, Christian Lévêque, Claire Debarnot, Pascale Marchot, Sofija Paneva, Dominique Debanne, Michael Russier, Michael Seagar, Sarosh Irani, Oussama El Far
Brain - A Journal of Neurology awac218 (2022)10.1093/brain/awac218
Report from the 27th (Virtual) Meeting on Toxinology, “Toxins: Mr Hyde or Dr Jekyll?”, Organized by the French Society of Toxinology, 9–10 December 2021
Daniel Ladant, Pascale Marchot, Sylvie Diochot, Gilles Prévost, Michel Popoff, Evelyne Benoit
Toxins 14:1-32 (2022)10.3390/toxins14020110
2021
Comparative mapping of selected structural determinants on the extracellular domains of cholinesterase-like cell-adhesion molecules.
Davide Comoletti, Laura Trobiani, Arnaud Chatonnet, Yves Bourne, Pascale Marchot
Neuropharmacology 184:108381 (2021)10.1016/j.neuropharm.2020.108381
2020
The neuroligins and the synaptic pathway in Autism Spectrum Disorder.
Laura Trobiani, Maria Meringolo, Tamara Diamanti, Yves Bourne, Pascale Marchot, Giuseppina Martella, Luciana Dini, Antonio Pisani, Antonella de Jaco, Paola Bonsi
Neuroscience and Biobehavioral Reviews 119:37-51 (2020)10.1016/j.neubiorev.2020.09.017
The Ig-like domain of Punctin/MADD-4 is the primary determinant for interaction with the ectodomain of neuroligin NLG-1
Semeli Platsaki, Xin Zhou, Bérangère Pinan-Lucarré, Vincent Delauzun, Haijun Tu, Pascal Mansuelle, Patrick Fourquet, Yves Bourne, Jean-Louis Bessereau, Pascale Marchot
Journal of Biological Chemistry 16267-16279. (2020)10.1074/jbc.RA120.014591
Report from the 26th Meeting on Toxinology, Bioengineering of Toxins, Organized by the French Society of Toxinology (SFET) and Held in Paris, France, 4-5 December 2019
Pascale Marchot, Sylvie Diochot, Michel R Popoff, Evelyne Benoit
Toxins 12:1-30 (2020)10.3390/toxins12010031
2019
An evolutionary perspective on the first disulfide bond in members of the cholinesterase-carboxylesterase (COesterase) family: Possible outcomes for cholinesterase expression in prokaryotes
Arnaud Chatonnet, Xavier Brazzolotto, Thierry Hotelier, Nicolas Lenfant, Pascale Marchot, Yves Bourne
Chemico-Biological Interactions 308:179-184 (2019)10.1016/j.cbi.2019.05.016
2018
Hot Spots for Protein Partnerships at the Surface of Cholinesterases and Related α/β Hydrolase Fold Proteins or Domains—A Structural Perspective
Yves Bourne, Pascale Marchot
Molecules 23 (2018)10.3390/molecules23010035
2017
The three-finger toxin fold: a multifunctional structural scaffold able to modulate cholinergic functions
Pascal Kessler, Pascale Marchot, Marcela Silva, Denis Servent
Journal of Neurochemistry 142:7-18 (2017)10.1111/jnc.13975
A Triad of Crystals Sheds Light on MDGA Interference with Neuroligation
Olivier Thoumine, Pascale Marchot
Neuron 95:729-732 (2017)10.1016/j.neuron.2017.08.001
Preface: Cholinergic Mechanisms
Marco Prado, Pascale Marchot, Israel Silman, Marco A.M. Prado
Journal of Neurochemistry 142:3-6 (2017)10.1111/jnc.14027
Cyclic imine toxins from dinoflagellates: a growing family of potent antagonists of the nicotinic acetylcholine receptors
Jordi Molgó, Pascale Marchot, Rómulo Aráoz, Evelyne Benoit, Bogdan I Iorga, Armen Zakarian, Palmer Taylor, Yves Bourne, Denis Servent
Journal of Neurochemistry 142:41-51 (2017)10.1111/jnc.13995
Natural genomic amplification of cholinesterase genes in animals
Arnaud Chatonnet, Nicolas Lenfant, Pascale Marchot, Murray E. Selkirk
Journal of Neurochemistry 142:73-81 (2017)10.1111/jnc.13990
2016
Relationships of human alpha/beta hydrolase fold proteins and other organophosphate-interacting proteins
Nicolas Lenfant, Yves Bourne, Pascale Marchot, Arnaud Chatonnet
Chemico-Biological Interactions 259:343-351 (2016)10.1016/j.cbi.2016.04.027
Steric and Dynamic Parameters Influencing In Situ Cycloadditions to Form Triazole Inhibitors with Crystalline Acetylcholinesterase
Yves Bourne, K. Barry Sharpless, Palmer Taylor, Pascale Marchot
Journal of the American Chemical Society 138:1611-1621 (2016)10.1021/jacs.5b11384
2015
Marine Macrocyclic Imines, Pinnatoxins A and G: Structural Determinants and Functional Properties to Distinguish Neuronal α7 from Muscle α12βγδ nAChRs.
Yves Bourne, Gerlind Sulzenbacher, Zoran Radić, Rómulo Aráoz, Morgane Reynaud, Evelyne Benoit, Armen Zakarian, Denis Servent, Jordi Molgó, Palmer Taylor, Pascale Marchot
Structure 23:1106-15 (2015)10.1016/j.str.2015.04.009
Crystal structure of snake venom acetylcholinesterase in complex with inhibitory antibody fragment Fab410 bound at the peripheral site - Evidence for open and closed states of a back door channel
Yves Bourne, Ludovic Renault, Pascale Marchot
Journal of Biological Chemistry 290:1522-1535 (2015)10.1074/jbc.M114.603902
2014
Special Issue on “freshwater and marine toxins”
Evelyne Benoit, César Mattei, Julien Barbier, Pascale Marchot, Jordi Molgó, Denis Servent
Toxicon 91:1-4 (2014)10.1016/j.toxicon.2014.11.217
Editorial : Special Issue on "freshwater and marine toxins".
Evelyne Benoit, César Mattei, Julien Barbier, Pascale Marchot, Jordi Molgó, Denis Servent
Toxicon 91:1-4 (2014)10.1016/j.toxicon.2014.11.217
The neuroligins and their neurexin ligands: from structure to function at the synapse
Yves Bourne, Pascale Marchot
Journal of Molecular Neuroscience 53:387-396 (2014)10.1007/s12031-014-0234-6
Tracking the origin and divergence of cholinesterases and neuroligins: the evolution of synaptic proteins
Nicolas Lenfant, Thierry Hotelier, Yves Bourne, Pascale Marchot, Arnaud Chatonnet
Journal of Molecular Neuroscience 53:362-369 (2014)10.1007/s12031-013-0194-2
2013
Editorial : Special issue on "toxins: from threats to benefits".
Marie-France Martin-Eauclaire, Evelyne Benoit, Pascale Marchot, Julien Barbier, Jordi Molgó, Denis Servent
Toxicon 75:1-2 (2013)10.1016/j.toxicon.2013.08.001
Molecular Characterization of Monoclonal Antibodies that Inhibit Acetylcholinesterase by Targeting the Peripheral Site and Backdoor Region
Yves Bourne, Ludovic Renault, Sosthène Essono, Grégoire Mondielli, Patricia Lamourette, Didier Boquet, Jacques Grassi, Pascale Marchot
PLoS ONE 8:e77226 (2013)10.1371/journal.pone.0077226
ESTHER, the database of the α/β-hydrolase fold superfamily of proteins: tools to explore diversity of functions
Nicolas Lenfant, Thierry Hotelier, Eric Velluet, Yves Bourne, Pascale Marchot, Arnaud Chatonnet
Nucleic Acids Research 41:423-429 (2013)10.1093/nar/gks1154
Proteins with an alpha/beta hydrolase fold: Relationships between subfamilies in an ever-growing superfamily.
Nicolas Lenfant, Thierry Hotelier, Yves Bourne, Pascale Marchot, Arnaud Chatonnet
Chemico-Biological Interactions 203:266-268 (2013)10.1016/j.cbi.2012.09.003
2012
Structural Insights into Antibody Sequestering and Neutralizing of Na+ Channel α-Type Modulator from Old World Scorpion Venom.
Igor P Fabrichny, Grégoire Mondielli, Sandrine Conrod, Marie-France Martin-Eauclaire, Yves Bourne, Pascale Marchot
Journal of Biological Chemistry 287:14136-48 (2012)10.1074/jbc.M111.315382
Hydrolase versus other functions of members of the alpha/beta-hydrolase fold superfamily of proteins.
Pascale Marchot, Arnaud Chatonnet
Protein and Peptide Letters 19:130-131 (2012)10.2174/092986612799080239
Enzymatic activity and protein interactions in alpha/beta hydrolase fold proteins: moonlighting versus promiscuity.
Pascale Marchot, Arnaud Chatonnet
Protein and Peptide Letters 19:132-143 (2012)10.2174/092986612799080284
2010
Conformational remodeling of femtomolar inhibitor-acetylcholinesterase complexes in the crystalline state.
Yves Bourne, Zoran Radić, Palmer Taylor, Pascale Marchot
Journal of the American Chemical Society 132:18292-300 (2010)10.1021/ja106820e
Structural insights into the exquisite selectivity of neurexin/neuroligin synaptic interactions.
Philippe Leone, Davide Comoletti, Géraldine Ferracci, Sandrine Conrod, Simon U Garcia, Palmer Taylor, Yves Bourne, Pascale Marchot
EMBO Journal 29:2461-71 (2010)10.1038/emboj.2010.123
Structural determinants in phycotoxins and AChBP conferring high affinity binding and nicotinic AChR antagonism.
Yves Bourne, Zoran Radic, Rómulo Aráoz, Todd T Talley, Evelyne Benoit, Denis Servent, Palmer Taylor, Jordi Molgó, Pascale Marchot
Proceedings of the National Academy of Sciences of the United States of America 107:6076-81 (2010)10.1073/pnas.0912372107
Structure-function relationships of the alpha/beta-hydrolase fold domain of neuroligin: A comparison with acetylcholinesterase.
Philippe Leone, Davide Comoletti, Palmer Taylor, Yves Bourne, Pascale Marchot
Chemico-Biological Interactions epub ahead of print (2010)10.1016/j.cbi.2010.01.030
Insecticide resistance through mutations in cholinesterases or carboxylesterases : data mining in the ESTHER database
Thierry Hotelier, Vincent Negre, Pascale Marchot, Arnaud Chatonnet
Journal of Pesticide Science 35:315-320 (2010)10.1584/jpestics.R10-10
2009
Structural determinants for interaction of partial agonists with acetylcholine binding protein and neuronal α7 nicotinic acetylcholine receptor
Ryan Hibbs, Gerlind Sulzenbacher, Jianxin Shi, Todd Talley, Sandrine Conrod, William Kem, Palmer Taylor, Pascale Marchot, Yves Bourne
EMBO Journal 28:3040-3051 (2009)10.1038/emboj.2009.227
2007
Structural Analysis of the Synaptic Protein Neuroligin and Its β-Neurexin Complex: Determinants for Folding and Cell Adhesion
Igor Fabrichny, Philippe Leone, Gerlind Sulzenbacher, Davide Comoletti, Meghan Miller, Palmer Taylor, Yves Bourne, Pascale Marchot
Neuron 56:979-991 (2007)10.1016/j.neuron.2007.11.013
2006
Substrate and product trafficking through the active center gorge of acetylcholinesterase analyzed by crystallography and equilibrium binding.
Yves Bourne, Zoran Radic, Gerlind Sulzenbacher, Esther Kim, Palmer Taylor, Pascale Marchot
Journal of Biological Chemistry 281:29256-67 (2006)10.1074/jbc.M603018200
Structural characterization of agonist and antagonist-bound acetylcholine-binding protein from Aplysia californica.
Scott B Hansen, Gerlind Sulzenbacher, Tom Huxford, Pascale Marchot, Yves Bourne, Palmer Taylor
Journal of Molecular Neuroscience 30:101-2 (2006)
Structural comparison of three crystalline complexes of a peptidic toxin with a synaptic acetylcholine recognition protein.
Yves Bourne, Scott B Hansen, Gerlind Sulzenbacher, Todd T Talley, Tom Huxford, Palmer Taylor, Pascale Marchot
Journal of Molecular Neuroscience 30:103-4 (2006)
2005
Structural insights into AChE inhibition by monoclonal antibodies
Ludovic Renault, Sosthène Essono, Marianick Juin, Didier Boquet, Jacques Grassi, Yves Bourne, Pascale Marchot
Chemico-Biological Interactions 157-158:397-400 (2005)10.1016/j.cbi.2005.10.073
A. niger protein “EstA”, perhaps a new electrotactin, defines a new class of fungal esterases within the α/β hydrolase fold superfamily
Yves Bourne, Alinda Hasper, Henri Chahinian, Ludovic Renault, Marianick Juin, Leo de Graaff, Pascale Marchot
Chemico-Biological Interactions 157-158:395-396 (2005)10.1016/j.cbi.2005.10.072
Structural insights into conformational flexibility at the peripheral site and within the active center gorge of AChE, Chem Biol Interact. 157-158, 159-65.
Yves Bourne, Z. Radic, Kolb H. C., Sharpless K. B., P. Taylor, Pascale Marchot
Chemico-Biological Interactions 157-158:159-65. (2005)
Structures of Aplysia AChBP complexes with nicotinic agonists and antagonists reveal distinctive binding interfaces and conformations
Scott B Hansen, Gerlind Sulzenbacher, Tom Huxford, Pascale Marchot, Palmer Taylor, Yves Bourne
EMBO Journal 24:3635-3646 (2005)10.1038/sj.emboj.7600828
Expression of the standard scorpion alpha-toxin AaH II and AaH II mutants leading to the identification of some key bioactive elements
C. Legros, B. Ceard, H. Vacher, Pascale Marchot, Bougis P. E., Martin-Eauclaire M. F.
BBA - Biochimica et Biophysica Acta 1723:91 99 (2005)
New friendly tools for users of ESTHER, the database of the alpha/beta-hydrolase fold superfamily of proteins,
L. Renault, V. Negre, T. Hotelier, Xavier Cousin, Pascale Marchot, Arnaud Chatonnet
Chemico-Biological Interactions 157-158:339-43. (2005)10.1016/j.cbi.2005.10.100
Crystal structure of a Cbtx-AChBP complex reveals essential interactions between snake alpha-neurotoxins and nicotinic receptors,
Yves Bourne, T. T. Talley, Hansen S. B., P. Taylor, Pascale Marchot
EMBO Journal 24:1512-1522 (2005)
2004
Aspergillus niger Protein EstA Defines a New Class of Fungal Esterases within the α/β Hydrolase Fold Superfamily of Proteins
Yves Bourne, Alinda A Hasper, Henri Chahinian, Marianick Juin, Leo H de Graaff, Pascale Marchot
Structure 12:677-687 (2004)10.1016/j.str.2004.03.005
Freeze-frame inhibitor captures acetylcholinesterase in a unique conformation
Y. Bourne, H. Kolb, Z. Radic, K. Sharpless, P. Taylor, Pascale Marchot
Proceedings of the National Academy of Sciences of the United States of America 101:1449-1454 (2004)10.1073/pnas.0308206100
ESTHER, the database of the alpha/beta-hydrolase fold superfamily of proteins
Thierry Hotelier, Ludovic Renault, Xavier Cousin, Vincent Negre, Pascale Marchot, Arnaud Chatonnet
Nucleic Acids Research 32:D145-D147 (2004)10.1093/nar/gkh141
2003
Structural insights into ligand interactions at the acetylcholinesterase peripheral anionic site
Yves Bourne, Palmer Taylor, Zoran Radic, Pascale Marchot
EMBO Journal 22:1-12 (2003)10.1093/emboj/cdg005
2002
Use of a purified and functional recombinant calcium-channel β4 subunit in surface-plasmon resonance studies
Sandrine Geib, Guillaume Sandoz, Kamel Mabrouk, Alessandra Matavel, Pascale Marchot, Toshinori Hoshi, Michel Villaz, Michel Ronjat, Raymond Miquelis, Christian Lévêque, Michel de Waard
Biochemical Journal 364:285-292 (2002)10.1042/bj3640285
Mechanism of Acetylcholinesterase Inhibition by Fasciculin: A 5-ns Molecular Dynamics Simulation
Kaihsu Tai, Tongye Shen, Richard Henchman, Yves Bourne, Pascale Marchot, J. Andrew Mccammon
Journal of the American Chemical Society 124:6153-6161 (2002)10.1021/ja017310h
2000
On the kaliotoxin and dendrotoxin binding sites on rat brain synaptosomes
N Tricaud, Pascale Marchot, M.F Martin-Eauclaire
Toxicon 38:1749-1758 (2000)10.1016/s0041-0101(00)00104-5
Immunocytochemical Localization and Crystal Structure of Human Frequenin (Neuronal Calcium Sensor 1)
Yves Bourne, Jens Dannenberg, Verena Pollmann, Pascale Marchot, Olaf Pongs
Journal of Biological Chemistry 276:11949-11955 (2000)10.1074/jbc.m009373200
1999
Conformational Flexibility of the Acetylcholinesterase Tetramer Suggested by X-ray Crystallography*
Yves Bourne, Jacques Grassi, Pierre E Bougis, Pascale Marchot
Journal of Biological Chemistry 274:30370-30376 (1999)
Electron paramagnetic resonance reveals altered topography of the active center gorge of acetylcholinesterase after binding of fasciculin to the peripheral site
Marjeta Šentjurc, Slavko Pečar, Jure Stojan, Pascale Marchot, Zoran Radić, Zoran Grubič
Biochimica et Biophysica Acta (BBA) - Protein Structure and Molecular Enzymology 1430:349-358 (1999)10.1016/s0167-4838(99)00018-7
Crystal Structure of Mouse Acetylcholinesterase
Yves Bourne, Palmer Taylor, Pierre E Bougis, Pascale Marchot
Journal of Biological Chemistry 274:2963-2970 (1999)10.1074/jbc.274.5.2963
L’interaction fasciculine-acétylcholinestérase
Pascale Marchot
Journal de la Société de Biologie 193:505-508 (1999)10.1051/jbio/1999193060505
1998
Inhibition of mouse acetylcholinesterase by fasciculin: Crystal structure of the complex and mutagenesis of fasciculin
Pascale Marchot, Yves Bourne, Claudine Prowse, Pierre Bougis, Palmer Taylor
Toxicon 36:1613-1622 (1998)10.1016/s0041-0101(98)00154-8
Residues at the Subunit Interfaces of the Nicotinic Acetylcholine Receptor That Contribute to α-Conotoxin M1 Binding
Naoya Sugiyama, Pascale Marchot, Chiaki Kawanishi, Hitoshi Osaka, Brian Molles, Steven Sine, Palmer Taylor
Molecular Pharmacology 53:787-794 (1998)10.1124/mol.53.4.787
Toxins selective for subunit interfaces as probes of nicotinic acetylcholine receptor structure
Palmer Taylor, Hitoshi Osaka, Brian Molles, Naoya Sugiyama, Pascale Marchot, Elizabeth Ackermann, Siobhan Malany, Joseph Mcardle, Steven Sine, Igor Tsigelny
Journal of Physiology - Paris 92:79-83 (1998)10.1016/S0928-4257(98)80142-3
1997
Expression and Activity of Mutants of Fasciculin, a Peptidic Acetylcholinesterase Inhibitor from Mamba Venom*
Pascale Marchot, Claudine N Prowse, Joan Kanter, Shelley Camp, Elizabeth J Ackermann, Zoran Radić, Pierre E Bougis, Palmer Taylor
Journal of Biological Chemistry 272:3502-3510 (1997)
1996
Soluble monomeric acetylcholinesterase from mouse: Expression, purification, and crystallization in complex with fasciculin
Pascale Marchot, Raimond B.G. Ravelli, Mia Raves, Yves Bourne, Daniel Vellom, Joan Kanter, Shelley Camp, Joel Sussman, Palmer Taylor
Protein Science 5:672-679 (1996)10.1002/pro.5560050411
Structure of fasciculin 2 from green mamba snake venom: evidence for unusual loop flexibility
Marie-Hélène Le Du, Pascale Marchot, D. Housset, P. Bougis, J. Navaza, Juan-Carlos Fontecilla-Camps
Acta crystallographica Section D : Structural biology [1993-...] 52:87-92 (1996)10.1107/S0907444995007517
1995
Structural bases for the specificity of cholinesterase catalysis and inhibition
Palmer Taylor, Zoran Radic, Natilie Hosea, Shelley Camp, Pascale Marchot, Harvey Berman
Toxicology Letters 82-83:453-458 (1995)10.1016/0378-4274(95)03575-3
Acetylcholinesterase Inhibition by Fasciculin: Crystal Structure of the Complex
Yves Bourne, Palmer Taylor, Pascale Marchot
Cell 83:503-512 (1995)10.1016/0092-8674(95)90128-0
Afaacytin, an alphabeta-fibrinogenase from Cerastes cerastes (Horned Viper) Venom, Activates Purified Factor X and Induces Serotonin Release from Human Blood Platelets
Fatirna Laraba-Djebari, Marie-France Martin-Eauclaire, Gerard Mauco, Pascale Marchot
European Journal of Biochemistry 233:756-765 (1995)10.1111/j.1432-1033.1995.756_3.x
Theoretical analysis of the structure of the peptide fasciculin and its docking to acetylcholinesterase
Harald van den Born, Zoran Radić, Pascale Marchot, Palmer Taylor, Igor Tsigelny
Protein Science 4:703-715 (1995)10.1002/pro.5560040410
1993
Binding of 125I-fasciculin to rat brain acetylcholinesterase. The complex still binds diisopropyl fluorophosphate
Pascale Marchot, Akila Khelif, Yong-Hua Ji, Pascal Mansuelle, Pierre E. Bougis
Journal of Biological Chemistry 268:12458-12467 (1993)
1992
1.9 A resolution structure of fasciculin 1, an anti-acetylcholinesterase toxin from green mamba snake venom
Marie-Hélène Le Du, Pascale Marchot, Pierre E Bougis, Juan-Carlos Fontecilla-Camps
Journal of Biological Chemistry 267:22122-22130 (1992)10.2210/pdb1fas/pdb
A fibrinogen-clotting serine proteinase from Cerastes cerastes (horned viper) venom with arginine-esterase and amidase activities. Purification, characterization and kinetic parameter determination
Fatima Laraba-Djebari, Marie-France Martin-Eauclaire, Pascale Marchot
Toxicon 30:1399-1410 (1992)10.1016/0041-0101(92)90515-7
1990
Neurotoxicité chez la souris de portions riches en cystéines des protéines Tat du virus visna et de VIH-1
Isabelle Gourdou, Kamel Mabrouk, Gordon Harkiss, Pascale Marchot, Neil Watt, Francis Hery, Robert Vigne
Comptes rendus de l’Académie des sciences. Série III, Sciences de la vie 311:149-55 (1990)
Homologues of a K+ channel blocker α-dendrotoxin: characterization of synaptosomal binding sites and their coupling to elevation of cytosolic free calcium concentration
Z.M. Muniz, G.R. Tibbs, Pascale Marchot, P. Bougis, D.G. Nicholls, J.O. Dolly
Neurochemistry International 16:105-112 (1990)10.1016/0197-0186(90)90130-L
1989
Crystals of fasciculin 2 from green mamba snake venom. Preparation and preliminary x-ray analysis
Marie Hélène Le Du, Pascale Marchot, Pierre E Bougis, Juan-C Fontecilla-Camps
Journal of Biological Chemistry 264:21401-21402 (1989)10.1016/S0021-9258(19)30094-8
1988
Localization of the toxic site of Naja mossambica cardiotoxins: small synthetic peptides express an in vivo lethality
Pascale Marchot, P.E. Bougis, B. Ceard, J. van Rietschoten, H. Rochat
Biochemical and Biophysical Research Communications 153:642-647 (1988)10.1016/s0006-291x(88)81143-4
Selective distinction at equilibrium between the two alpha-neurotoxin binding sites of Torpedo acetylcholine receptor by microtitration
Pascale Marchot, Paule Frachon, Pierre Bougis
European Journal of Biochemistry 174:537-542 (1988)10.1111/j.1432-1033.1988.tb14132.x
Selective loss of binding sites for the iodinated alpha-neurotoxin I from Naja mossambica mossambica venom upon enzymatic deglycosylation of Torpedo electric organ membranes
Saadia Zeghloul, Pascale Marchot, Pierre Bougis, Catherine Ronin
European Journal of Biochemistry 174:543-550 (1988)10.1111/j.1432-1033.1988.tb14133.x
1987
Monitoring the purification by high-performance liquid chromatography of cardiotoxins from Naja mossambica mossambica using phase-sensitive two-dimensional nuclear magnetic resonance
Gottfried Otting, Pascale Marchot, Pierre E Bougis, Hervé Rochat, Kurt Wüthrich
European Journal of Biochemistry 168:603-607 (1987)10.1111/j.1432-1033.1987.tb13459.x
In vivo synergy of cardiotoxin and phospholipase A2 from the elapid snake Naja mossambica mossambica
Pierre E Bougis, Pascale Marchot, Hervé Rochat
Toxicon 25:427-431 (1987)10.1016/0041-0101(87)90076-6
Use of high performance liquid chromatography to demonstrate quantitative variation in components of venom from the scorpion Androctonus australis hector
M.F Martin, Hervé Rochat, Pascale Marchot, Pierre E Bougis
Toxicon 25:569-573 (1987)10.1016/0041-0101(87)90293-5
1986
Characterization of elapidae snake venom components using optimized reverse-phase high-performance liquid chromatographic conditions and screening assays for alpha-neurotoxin and phospholipase A2 activities
Pierre E Bougis, Pascale Marchot, Hervé Rochat
Biochemistry 25:7235-43 (1986)10.1021/bi00370a070



